题目内容
下列化学用语正确的是( )
A、Cl-的结构示意图: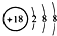 | ||
| B、光导纤维主要成分的化学式:Si | ||
| C、1H2、2H2、3H2互为同位素 | ||
D、质子数为53,中子数为78的碘原子:
|
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氯离子的核电荷数为17,氯原子标出氯离子,核电荷数不会变化;
B.光导纤维的主要成分为二氧化硅;
C.同位素的研究对象为原子,1H2、2H2、3H2为氢气,为同一种物质;
D.质量数=质子数+中子数,元素符号的左上角表示的是质量数,左下角表示质子数.
B.光导纤维的主要成分为二氧化硅;
C.同位素的研究对象为原子,1H2、2H2、3H2为氢气,为同一种物质;
D.质量数=质子数+中子数,元素符号的左上角表示的是质量数,左下角表示质子数.
解答:
解:A.氯离子的核电荷数为17,核外电子总数为18,氯离子结构示意图为: ,故A错误;
,故A错误;
B.光导纤维的主要成分表示Si,应该为二氧化硅,化学式为:SiO2,故B错误;
C.同种元素的不同原子互为同位素,1H2、2H2、3H2为同一种物质,都是分子,不属于同位素,故C错误;
D.质子数为53,中子数为78的碘原子,其质量数为131,该碘原子可以表示为:53131I,故D正确;
故选D.
 ,故A错误;
,故A错误;B.光导纤维的主要成分表示Si,应该为二氧化硅,化学式为:SiO2,故B错误;
C.同种元素的不同原子互为同位素,1H2、2H2、3H2为同一种物质,都是分子,不属于同位素,故C错误;
D.质子数为53,中子数为78的碘原子,其质量数为131,该碘原子可以表示为:53131I,故D正确;
故选D.
点评:本题考查了离子结构示意图、元素符号、同位素的判断,题目难度不大,注意掌握同位素、离子结构示意图、元素符号的表示方法,明确同位素与同素异形体、同分异构体之间的区别.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
一种新型绿色电池-燃料电池,是把H2、CO、CH4气体和空气不断输入直接氧化,使化学能转变为电能,它被称为21世纪的绿色发电站,这三种气体可以作为燃料电池所需燃料的理由是( )
| A、都是无毒无害气体 |
| B、在自然界都大量存在 |
| C、都可以燃烧并放出大量的热 |
| D、燃烧产物均为CO2和H2O |
设 NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、16g CH4中含有10NA个电子 |
| B、1mol?L-1NaCl溶液含有NA个Na+ |
| C、1mol Cu和足量稀硝酸反应产生NA个NO分子 |
| D、常温常压下,22.4L CO2中含有NA个CO2分子 |
同温同压下,1molHe和1molCH4具有相同的( )
| A、原子数 | B、质子数 |
| C、质量 | D、体积 |
下列说法中正确的一组是( )
| A、H2和D2互为同位素 |
B、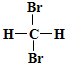 和 和 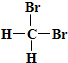 互为同分异构体 互为同分异构体 |
C、碳链为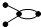 与 与 的烃为同系物 的烃为同系物 |
| D、金刚石、石墨互为同素异形体 |
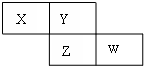 X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )| A、气态氢化物的稳定性:X>Y |
| B、Z元素的氧化物对应的水化物一定是一种强酸 |
| C、X、Y、Z原子半径的大小顺序:X>Y>Z |
| D、X的气态氢化物与W的气态氢化物可以相互反应 |
对25℃时的醋酸溶液,若采用下列不同的措施:
(1)加入NaOH固体(2)加入CaCO3固体 (3)加等体积的水稀释 (4)加热醋酸溶液使温度上升10℃(5)加入醋酸钠晶体 (6)加入盐酸,其中能使醋酸电离度增大的有( )
(1)加入NaOH固体(2)加入CaCO3固体 (3)加等体积的水稀释 (4)加热醋酸溶液使温度上升10℃(5)加入醋酸钠晶体 (6)加入盐酸,其中能使醋酸电离度增大的有( )
| A、(1)(3)(4) |
| B、(1)(2)(3)(4) |
| C、(1)(3)(4)(5) |
| D、(1)(2)(3)(4)(5) |
 实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液480mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液480mL.根据这两种溶液的配制情况回答下列问题: