题目内容
8.25℃时,有100mL 0.1mol/LNaHB溶液pH=1(1)若向该溶液中加V1 mL水,使溶液pH变为2,则V1=900mL (设溶液体积无变化).
(2)25℃时此溶液和某浓度氨水pH之和为14,二者等体积混合后溶液中离子浓度由大到小的顺序为:c(NH4+)>c(Na+)=c(B2-)>c(OH-)>c(H+).
分析 (1)0.1mol/LNaHB溶液pH=1,氢离子浓度为0.1mol/L,说明NaHB在溶液中完全电离出氢离子;稀释后氢离子浓度为0.01mol/L,然后根据稀释定律计算出加入水的体积;
(2)25℃时此溶液和某浓度氨水pH之和为14,氨水的pH=14-1=13,由于氨水为弱碱,二者等体积混合后氨水过量,溶液呈碱性,则:c(OH-)>c(H+),据此判断各离子浓度大小.
解答 解:(1)0.1mol/LNaHB溶液pH=1,氢离子浓度为0.1mol/L,说明NaHB在溶液中完全电离出氢离子,
若向该溶液中加V1 mL水,使溶液pH变为2,氢离子浓度为0.01mol/L,
稀释过程中氢离子的物质的量不变,则满足:0.1mol/L×0.1L=0.01mol/L×(0.1L+V1×10-3L),
解得:V1=900mL,
故答案为:900;
(2)25℃时此溶液和某浓度氨水pH之和为14,氨水的pH=14-1=13,由于氨水为弱碱,二者等体积混合后氨水过量,溶液呈碱性,则c(OH-)>c(H+),根据物料守恒可得c(Na+)=c(B2-),反应后溶质离子浓度大小为:c(NH4+)>c(Na+)=c(B2-)>c(OH-)>c(H+),
故答案为:c(NH4+)>c(Na+)=c(B2-)>c(OH-)>c(H+).
点评 本题考查了溶液pH计算、离子浓度大小比较,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握pH的计算方法,试题培养了学生学生的分析能力及化学计算能力.

练习册系列答案
相关题目
19.下列有关金属的说法中,正确的是( )
①铝合金门窗耐腐蚀 ②钠着火用水扑灭 ③KSCN溶液可以检验Fe3+④缺钙会引起骨质疏松,缺铁会引起贫血 ⑤青铜、不锈钢、硬铝都是合金.
①铝合金门窗耐腐蚀 ②钠着火用水扑灭 ③KSCN溶液可以检验Fe3+④缺钙会引起骨质疏松,缺铁会引起贫血 ⑤青铜、不锈钢、硬铝都是合金.
| A. | ①③④ | B. | ②③④⑤ | C. | ①③④⑤ | D. | ①②⑤ |
16.在水溶液中能大量共存的一组离子是( )
| A. | H+、SO42-、Na+、SiO32- | B. | Ag+、Fe3+、Cl-、SO42- | ||
| C. | H+、I-、Cl-、NO3- | D. | K+、SO42-、Mg2+、NO3- |
20.将Na2O2投入FeCl3溶液中,可观察到的实验现象是( )
| A. | 有白色沉淀生成 | |
| B. | 有红棕色沉淀生成 | |
| C. | 没有沉淀生成 | |
| D. | 既有红褐色沉淀生成又有无色气体产生 |
18.A、B、C、D、E、F六种化合物,其中A、B、C、D、E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC.
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
写出B与稀H2SO4反应的离子方程式S2O32-+2H+=S↓+SO2↑+H2O,写出②中离子反应方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子),XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol.
(4)化合物D和E相互转化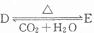 ,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC.
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
| ①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
| ②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
| ③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子),XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol.
(4)化合物D和E相互转化
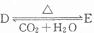 ,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O. 
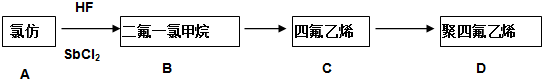
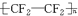 .
.