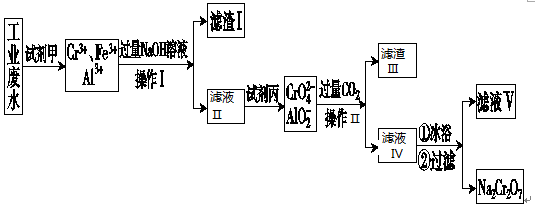
题目内容
1. pH=2的HA、HB两种酸溶液各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图所示,其中A代表酸HA,B代表酸HB.下列说法正确的是( )
pH=2的HA、HB两种酸溶液各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图所示,其中A代表酸HA,B代表酸HB.下列说法正确的是( )| A. | 稀释前两酸溶液的物质的量浓度相等 | |
| B. | 稀释后,HA酸溶液的酸性比HB酸溶液强 | |
| C. | a=5时,HA是强酸,HB是弱酸 | |
| D. | 若有等浓度的NaA溶液和NaB溶液,则溶液的碱性NaA>NaB |
分析 由图可知,稀释相同的倍数,HA的变化大,则HA的酸性比HB的酸性强,溶液中氢离子浓度越大,酸性越强,对于一元强酸来说c(酸)=c(H+),但对于一元弱酸,c(酸)>c(H+),以此来解答.
解答 解:A.因HA、HB酸的强弱不同,且均为一元酸,故当溶液的pH相同即氢离子浓度相同时,两酸溶液的物质的量浓度不同,且c(HB)>c(HA),故A错误;
B.稀释后,HA溶液的pH比HB大,故HA中氢离子浓度比HB中的小,则酸性更弱,故B错误;
C.由图可知,若a=5,则HA稀释1000倍时溶液的pH变化为3,符合强酸的稀释规律,则HA是强酸,HB的pH变化小,则HB为弱酸,故C正确;
D.由于酸性HA强于HB,根据酸越弱,则对应的盐的水解程度越大,故等浓度的NaA的水解程度小于NaB,即溶液的碱性NaA小于NaB,故D错误;
故选C.
点评 本题考查酸的稀释及图象,题目难度中等,侧重于学生的分析能力的考查,明确强酸在稀释时pH变化程度大及酸的浓度与氢离子的浓度的关系是解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.一定温度下,在三个体积均为1.0L 的恒容密闭容器中发生反应:2A(g)?B(g)+C(g)△H
下列说法不正确的是( )
| 容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| A(g) | B(g) | C(g) | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
| A. | 该反应的正反应为△H<0 | |
| B. | 207℃,K=4 | |
| C. | 达到平衡时,容器Ⅰ中的A体积分数与容器Ⅱ中的相同 | |
| D. | 容器Ⅰ中反应到达平衡所需时间比容器Ⅲ中的短 |
11.下列物质含有离子键的是( )
| A. | H2 | B. | NaCl | C. | HCl | D. | H2O |
16.下列说法正确的是( )
| A. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一有机反应类型 | |
| B. | 单质硅是将太阳能转化为电能的常用材料 | |
| C. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| D. | 合成纤维和光导纤维都是新型无机非金属材料 |
6.下列物质中,属于离子化合物的是( )
| A. | HCl | B. | NH4Cl | C. | NO | D. | C6H12O6(葡萄糖) |
13.下列物质的分子中,键角最小的是( )
| A. | NH3 | B. | SO3 | C. | H2O | D. | CCl4 |
10.最近我国全球首次海域试开采可燃冰圆满成功.与可燃冰释放出的气体成分相同的是( )
| A. | 天然气 | B. | 水煤气 | C. | 裂解气 | D. | 焦炉煤气 |