题目内容
下列叙述正确的是( )
| A、1 mol H2O的质量为18g/mol |
| B、CH4的摩尔质量为16g |
| C、3.01×1023个SO2分子的质量为32g |
| D、摩尔是国际单位制中的一个基本物理量 |
考点:摩尔质量,物质的量的单位--摩尔
专题:化学用语专题
分析:A、质量单位为g;
B、摩尔质量单位为g/mol;
C、依据n=
=
计算分析;
D、物质的量是国际单位制中的一个基本物理量,单位为mol;
B、摩尔质量单位为g/mol;
C、依据n=
| N |
| NA |
| m |
| M |
D、物质的量是国际单位制中的一个基本物理量,单位为mol;
解答:
解:A、质量单位为g,1 mol H2O的质量为18g,故A错误;
B、摩尔质量单位为g/mol,CH4的摩尔质量为16g/mol,故B错误;
C、依据n=
=
计算分析,3.01×1023个SO2分子的质量=
mol×64g/mol=32g,故C正确;
D、物质的量是国际单位制中的一个基本物理量,单位为mol,故D错误;
故选C.
B、摩尔质量单位为g/mol,CH4的摩尔质量为16g/mol,故B错误;
C、依据n=
| N |
| NA |
| m |
| M |
| 3.01×1023 |
| 6.02×1023 |
D、物质的量是国际单位制中的一个基本物理量,单位为mol,故D错误;
故选C.
点评:本题考查了摩尔质量单位和概念分析,物质的量的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列表示错误的是( )
| A、1mol O |
| B、1mol氧 |
| C、1mol O2- |
| D、1mol O2 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、含有NA个氮原子的氮气在标准状况下的体积约为22.4 L |
| B、标准状况下,11.2 L H2O含有的分子数为0.5NA |
| C、在常温常压下,11.2 L Cl2含有的分子数为0.5NA |
| D、25℃,1.01×105Pa,64 g SO2中含有的原子数为3NA |
新能源又称非常规能源.是指传统能源之外的各种能源形式.指刚开始开发利用或正在积极研究、有待推广的能源,如太阳能、地热能、风能、海洋能、生物质能和核聚变能等.下列有关新能源的说法不正确的是( )
| A、新能源与化石能源相比最直接的好处就是环境污染少 |
| B、利用晶体硅制作的太阳能电池可将太阳能直接转换为电能,实现太阳能的利用 |
| C、氢能是一种清洁的二次能源.可用电解水制氢的方法获取大量氢气实现能源的绿色化 |
| D、解决能源危机的方法是开源节流,即开发新能源和节约现有能源,提高原料的利用率 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L氧气做氧化剂时转移的电子数一定是4NA |
| B、1mol硝基(-NO2)与NA个二氧化氮(NO2)分子所含的电子数相等 |
| C、80 mL 12 mol/L的浓盐酸与足量MnO2反应,生成的Cl2分子数目为0.24NA |
| D、氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
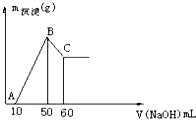 把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示,下列叙述不正确的是( )
把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示,下列叙述不正确的是( )| A、盐酸的物质的量浓度为0.5mol?L-1 |
| B、合金中铝的物质的量为0.01mol |
| C、合金中镁的物质的量为0.005mol |
| D、B点与C点沉淀的物质的量之比为2:1 |
配制一定物质的量浓度的NaOH溶液时,会对实验结果造成影响的是( )
①定容时,加水超过了刻度线,再用胶头滴管将过线的液体吸出
②定容时观察液面俯视
③有少量NaOH溶液残留在烧杯中
④容量瓶中原来有少量蒸馏水.
①定容时,加水超过了刻度线,再用胶头滴管将过线的液体吸出
②定容时观察液面俯视
③有少量NaOH溶液残留在烧杯中
④容量瓶中原来有少量蒸馏水.
| A、①②④ | B、①②③ |
| C、①② | D、②③④ |
沼气是一种能源,它的主要成分是CH41.6gCH4完全燃烧生成CO2和液态水时,放出89kJ热量,则下列热化学方程式中正确的是( )
| A、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=+890kJ?mol-1 | ||||
| B、CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890kJ?mol-1 | ||||
| C、CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ?mol-1 | ||||
D、
|