题目内容
17.将2.44g BaCl2•xH2O配成100mL溶液.25mL此溶液中的Cl-恰好能与50mL 0.1mol•L-1的AgNO3溶液完全反应.计算:(1)此溶液中溶质的物质的量浓度
(2)BaCl2•xH2O中的x的值.
分析 (1)发生反应Ag++Cl-=AgCl↓,据此计算25mL溶液中n(Cl-),而溶液中c(BaCl2)=$\frac{1}{2}$c(Cl-),据此分析;
(2)根据M=$\frac{m}{n}$计算BaCl2•XH2O摩尔质量,进而计算X的值.
解答 解:(1)50ml 0.1mol/L的AgNO3溶液中n(Ag+)=0.05L×0.1mol/L=0.005mol,由Ag++Cl-=AgCl↓可知,所以25mL氯化钡溶液中n(Cl-)=0.005mol,而溶液中c(BaCl2)=$\frac{1}{2}$c(Cl-)=$\frac{1}{2}$×$\frac{0.005mol}{0.025L}$=0.1mol/L.答:溶液中溶质的物质的量浓度为0.1moL/L;
(2)由于2.44克的BaCl2•XH2O配成100mL溶液,而溶液的浓度为0.1mol/L,故BaCl2•XH2O的物质的量为0.01moL,故其摩尔质量=$\frac{2.44g}{0.01mol}$=224g/mol,故244=18x+208,解得x=2.
答:BaCl2•xH2O中的x的值为2.
点评 本题考查物质的量浓度有关计算、离子方程式有关计算等,比较基础,关键是根据离子方程式确定氯离子的物质的量.

练习册系列答案
相关题目
7.下列每组中各有三对物质,它们都能用分液漏斗分离的是( )
| A. | 乙酸乙酯和水,酒精和水,植物油和水 | |
| B. | 四氯化碳和水,溴苯和苯,硝基苯和水 | |
| C. | 甘油和水,乙酸和水,乙酸和乙醇 | |
| D. | 汽油和水,苯和水,己烷和水 |
8.下列对有机物结构或性质的描述中错误的是( )
| A. | 一定条件下,Cl2可与甲苯的苯环或侧链发生取代反应 | |
| B. | 1 mol乙烷和丙烯混合物完全燃烧生成3 molH2O | |
| C. | 用核磁共振氢谱不能鉴别1-丙醇和2-丙醇 | |
| D. | 邻二溴苯仅有一种空间结构,证明苯分子中不存在单双键交替的结构 |
5.在“冰→液体水→氢气和氧气”的变化过程中,微粒间被破坏的作用力依次是( )
| A. | 范德华力、范德华力 | B. | 范德华力、共价键 | ||
| C. | 共价键、范德华力 | D. | 共价键、共价键 |
12.同一主族的两种元素的原子序数之差不可能是( )
| A. | 2 | B. | 16 | C. | 26 | D. | 46 |
2.在某一化学反应A+3B═2C+D中,反应物A的浓度在20s内由1.0mol/L变成0.2mol/L,则在这20s内用C表示的平均反应速率为( )
| A. | v(C)=0.01 mol/(L•s) | B. | v(C)=0.8 mol/(L•s) | C. | v(C)=0.04 mol/(L•s) | D. | v(C)=0.08 mol/(L•s) |
9.下列叙述中,金属A的活泼性肯定比金属B的活泼性强的是( )
| A. | 1 mol A 与足量的酸反应生成的H2比1 mol B生成的H2多 | |
| B. | A原子电子层数比B原子的电子层数多 | |
| C. | 常温时,A能从水中置换出氢,而B不能 | |
| D. | A原子的最外层电子数比B原子的最外层电子数少 |
7.25℃时,下列溶液中微粒的物质的量浓度关系不正确的是( )
| A. | 0.1mol•L-1NaHC2O4溶液(pH=5.5):c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| B. | 0.1mol•L-1NaHS溶液:c(OH-)+c(S2-)=c(H+)+c(H2S) | |
| C. | 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.1mol•L-1CH3COOH溶液和0.1mol•L-1CH3COONa溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
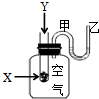 为了研究化学反应X+Y=Z的能量变化情况,某同学设计了如图所示装置.当向盛有X的试管中滴加试剂Y时,看到U型管中甲处液面下降乙处液面上升.试回答下列问题:
为了研究化学反应X+Y=Z的能量变化情况,某同学设计了如图所示装置.当向盛有X的试管中滴加试剂Y时,看到U型管中甲处液面下降乙处液面上升.试回答下列问题: