题目内容
12.2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ•mol-1、CO(g)+O2(g)=CO2(g)△H=-283kJ•mol-1某H2和CO的混合气体完全燃烧时放出113.74kJ热量,同时生成3.6g液态水,则原混合气体的H2和CO的物质的量之比( )| A. | 2:1 | B. | 1:2 | C. | 1:1 | D. | 2:3 |
分析 水的物质的量为$\frac{3.6g}{18g/mol}$=0.2mol,由2H2+O2═2H2O可知,n(H2)=n(H2O)=0.2mol,由2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1可知0.2molH2燃烧放出的热量为57.16KJ,
则CO燃烧放出的热量为113.74KJ-57.16KJ=56.58KJ,
结合热化学方程式中物质的量与热量成正比计算.
解答 解:水的物质的量为$\frac{3.6g}{18g/mol}$=0.2mol,由2H2+O2═2H2O可知,n(H2)=n(H2O)=0.2mol,由2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1可知0.2molH2燃烧放出的热量为57.16KJ,
则CO燃烧放出的热量为113.74KJ-57.16KJ=56.58KJ,
设混合气体中CO的物质的量为x,则
CO(g)+O2(g)=CO2(g)△H=-283kJ•mol-1
1 283KJ
x 56.58KJ
$\frac{1}{x}$=$\frac{283kJ}{56.58kJ}$,解得x=0.2mol,即n(CO)=0.20mol,
原混合气体中H2和CO的物质的量均为0.2mol,H2和CO的物质的量之比为1:1,
故选C.
点评 本题考查热化学方程式的计算,为高频考点,把握物质的量与热量的关系为解答的关键,侧重分析与计算能力的考查,注意混合物中只有氢气燃烧生成水,题目难度不大.

练习册系列答案
相关题目
2.下表各组物质在适当条件均可反应,其中气体产物成分可能不唯一的是( )
| A. | 浓硫酸与铜 | B. | 浓硝酸与铜 | C. | 浓盐酸与MnO2 | D. | 浓氨水与CaO |
3.将某些化学知识用图象表示,可以收到直观、简明的效果.下列图象所表示的化学知识中,明显不正确的是( )
| A. |  分散系的分类 | |
| B. | 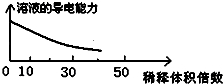 醋酸稀释 | |
| C. | 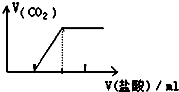 向Na2CO3溶液中逐滴滴入盐酸 | |
| D. | 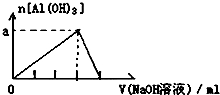 向AlCl3溶液中滴加过量的NaOH溶液 |
20.将1.95g锌粉加入到200mL 0.1mol•L-1的MO2+溶液中,恰好完全反应,其他物质忽略,则还原产物可能是( )
| A. | M2+ | B. | M | C. | M3+ | D. | MO2+ |
17.在实验室从自来水制取蒸馏水的实验中,下列说法错误的是( )
| A. | 烧瓶中要放入碎瓷片防止暴沸 | |
| B. | 不用温度计 | |
| C. | 冷凝水应该是下进上出,与蒸汽的流向相反 | |
| D. | 开始蒸馏时,应该先加热,再开冷凝水;蒸馏完毕,应该先关冷凝水再撤酒精灯 |
4.下列各组离子在水溶液中能大量共存的是( )
| A. | K+、HCO3-、CO32-、Br- | B. | SO32-、HSO3-、OH-、K+ | ||
| C. | Fe3+、Cu2+、NO3-、SO32- | D. | H+、Na+、NO3-、Fe2+ |
11.与氢气反应的热化学方程式是
①I2(g)+H2(g)?2HI(g)△H=-9.48KJ•mol-1
②I2(s)+H2(g)?2HI(g)△H=+26.48KJ•mol-1
下列说法正确的是( )
①I2(g)+H2(g)?2HI(g)△H=-9.48KJ•mol-1
②I2(s)+H2(g)?2HI(g)△H=+26.48KJ•mol-1
下列说法正确的是( )
| A. | ①的产物比②的产物稳定 | |
| B. | I2(s)=I2(g)△H=+17.00KJ•mol-1 | |
| C. | ②的反应物总能量比①的反应物总能量低 | |
| D. | 1molI2(g)中通入1molH2(g),发生反应时放热9.48KJ |

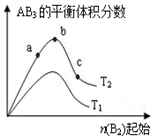 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据如图判断:
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据如图判断: