题目内容
9.依据表判断CH3CH3→CH2=CH2+H2的反应热为( )| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ•mol1) | 414.4 | 615.3 | 347.4 | 435.3 |
| A. | +125.6 kJ•molˉ1 | B. | -125.6 kJ•molˉ1 | C. | +46.1 kJ•molˉ1 | D. | -46.1 kJ•molˉ1 |
分析 根据反应热=反应物的键能之和-生成物的键能之和进行计算,1molCH3CH3中含有6molC-H,1molC-C,CH2=CH2中含有4molC-H,1molC=C,1molH2含有1molH-H.
解答 解:CH3CH3→CH2=CH2+H2,1molCH3CH3中含有6molC-H,1molC-C,CH2=CH2中含有4molC-H,1molC=C,1molH2含有1molH-H,反应热=反应物的键能之和-生成物的键能之和,所以该反应的反应热=347.4+6×414.4-615.3-414.4×4-435.3=+125.6kJ/mol,
故选A.
点评 本题考查学生对反应热的计算,题目难度不大,注意掌握反应热=反应物的键能之和-生成物的键能之和.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.将下列选项中的物质加人(或通入)氢硫酸溶液中,可使反应后溶液酸性最终增强的是( )
| A. | 氯气 | B. | 氢氧化钠 | C. | 硫酸钠 | D. | 二氧化硫 |
14.某一元弱酸HA的相对分子质量为M.在t℃时,将ag HA完全溶解于水中,得V mL饱和溶液,测得该溶液的密度为ρ g/cm3,其中溶液pH=b.下列叙述中,错误的是( )
| A. | t℃时,HA的Ka=10-2b/1000a/MV | |
| B. | 物质的量浓度:c(HA)=1000a/MV mol•L-1 | |
| C. | t℃时,HA的溶解度:S=100a/ρV g | |
| D. | HA的质量分数:ω(HA)=(a/ρV)×100% |
1.乌头酸的结构简式如图所示,下列关于乌头酸的说法错误的是( )


| A. | 分子式为C6H6O6 | |
| B. | 乌头酸能使酸性高锰酸钾溶液褪色 | |
| C. | 含1 mol乌头酸的溶液最多可消耗3 mol NaOH | |
| D. | 乌头酸能发生水解反应和加成反应 |
18.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 在密闭容器中,加入1.5mol H2和0.5mol N 2充分反应后,可得到NH3分子数为NA | |
| B. | 常温下,pH=2的醋酸溶液中所含H+的数目为0.01NA | |
| C. | 1L 0.1mol•L-1 AlCl3的溶液中所含Al3+的数目为0.1NA | |
| D. | 精炼铜时,阴极质量增加6.4g,则电路中转移的电子数为0.2NA |
19.将Cu片放入0.1mol/LFeCl3溶液中,反应一定时间后取出Cu片,所得溶液Q中的c(Fe3+):c(Fe2+)=2:3,下列有关说法中正确的是( )
| A. | 反应中转移电子为0.04 mol | B. | Q中n(Cu2+):n(Fe2+)=1:2 | ||
| C. | 溶液Q比原溶液增重了 1.28 g | D. | 3c(Fe3+)+2c(Fe2+)+2c(Cu2+)=0.1 mol/L |

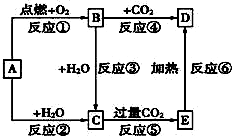 如图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.已知A在空气中燃烧生成淡黄色固体(部分产物已略去).
如图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.已知A在空气中燃烧生成淡黄色固体(部分产物已略去). 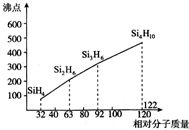 太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.
太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.