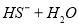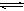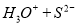��Ŀ����
��8�֣���25��ʱ������HA���MOH��������.
��1����0.01mol/L��ǿ��HA��0.01mol/Lǿ��MOH��ϣ���������Һ�� ������ԡ��������ԡ����ԡ�����ͬ���÷�Ӧ�����ӷ���ʽΪ
��2����pH=3��ǿ��HA��pH=11������MOH��ϣ���������Һ�� �������ǣ�
��3����0.01mol/L��ǿ��HA��0.01mol/L����MOH��ϣ���������Һ�� ��������һ��������ӷ���ʽ��
��1������ H++OH-=H2O
��2������ ��HA�� ��MOH�кͺ��������������OH-(2��)
��3�� ���� M++H2O MOH+H+(2��)
MOH+H+(2��)
��������
�����������1����0.01mol/L��ǿ��HA��0.01mol/Lǿ��MOH�������ϣ������ǡ����ȫ��Ӧ����ǿ��ǿ���Σ��ᷢ��ˮ�ⷴӦ�����������Һ�����ԣ��÷�Ӧ�����ӷ���ʽΪH++OH-=H2O����2����pH=3��ǿ��HA��pH=11������MOH�������ϣ���������ֵ��룬�����������IJ���ǡ����ȫ�кͣ�δ����IJ��ֻ�����������OH-,��������ʹ������Һ�Լ��ԣ���3����0.01mol/L��ǿ��HA��0.01mol/L����MOH�������ϣ������ǡ����ȫ��Ӧ����ǿ�������Ρ�����������������������ӷ���ˮ�ⷴӦ����ˮ���������OH-������ʹ��Һ�е�c(H+)> c(OH-)�����������Һ�����ԡ�������һ��������ӷ���ʽ��M++H2O MOH+H+��
MOH+H+��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���һ���ܱ���������X��Y��Z��Q�������ʣ���һ�������½��з�Ӧ��һ��ʱ����÷�Ӧǰ��������������ұ��� ����ܱ������з�����ѧ��Ӧ�Ļ������Ϳ����ǣ� ��
����ܱ������з�����ѧ��Ӧ�Ļ������Ϳ����ǣ� ��
���� | X | Y | Z | Q |
��Ӧǰ����/g | 20 | 20 | 20 | 20 |
��Ӧ������/g | 20 | 30 | 16 | 14 |
A���ֽⷴӦ B�����Ϸ�Ӧ C���û���Ӧ D�����ֽⷴӦ
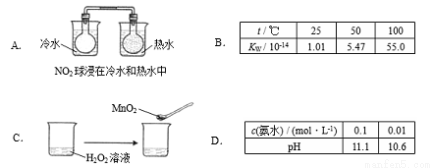
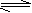 pC(g)+qD(g)����5min��ﵽƽ�⣬��ô�ʱA��Ũ�ȼ�����a mol/L��ͬʱC��Ũ��������2a/3 mol/L���ֲ��ƽ����Ӧ����v(C)=2v(B)���ﵽƽ����������¶Ȳ��䣬����ϵ��ѹ��ƽ�ⲻ�ƶ�����ô�÷�Ӧ�ɱ�ʾΪ�� ��
pC(g)+qD(g)����5min��ﵽƽ�⣬��ô�ʱA��Ũ�ȼ�����a mol/L��ͬʱC��Ũ��������2a/3 mol/L���ֲ��ƽ����Ӧ����v(C)=2v(B)���ﵽƽ����������¶Ȳ��䣬����ϵ��ѹ��ƽ�ⲻ�ƶ�����ô�÷�Ӧ�ɱ�ʾΪ�� �� 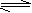 3C(g)+5D(g) B��3A(g)+ B(g)
3C(g)+5D(g) B��3A(g)+ B(g)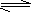 2C(g)+2D(g)
2C(g)+2D(g)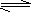 2C(g)+ D(g) D��A(g)+ 3B(g)
2C(g)+ D(g) D��A(g)+ 3B(g)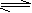 2C(g)+2D(g)
2C(g)+2D(g) 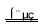 2OH- +Cl2�� +H2��
2OH- +Cl2�� +H2��