题目内容
根据反应框图填空,已知反应①~⑤均为工业生产及应用中常见反应,其中B、G、I、J、L均为常见单质,B、D、J、L为气体。A是工业生产F的重要矿石原料的主要成份,其相对分子质量为120,M为海水中含量最多的无机盐。
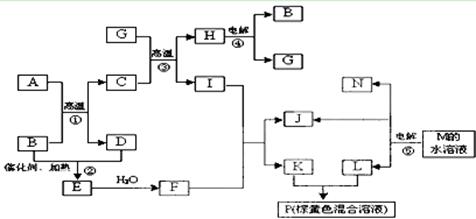
(1)I元素在元素周期表中的位置 ;M中阴离子的结构示意图: 。
(2)固体A中所包含的化学键与固体Na2O2类似,则A的电子式为 。
(3)写出下列化学反应的离子方程式:
① 溶液P与KSCN溶液:_____________________________________ ___;
② G与N的反应:______________________________________ __________;
③ K与L的反应:___________________________________ _____________。
(4)已知每生成16 gD,放出106.5 kJ热量,则反应①的热化学方程式为:
(1)第四周期第Ⅷ族;+19 2 8 8 。
(2) FeS2
(3)写出下列化学反应的离子方程式:
①Fe3+ + 3SCN- = Fe(SCN)3
②2Al + 2OH- +2H2O == 2AlO2- + 3H2
③2Fe2+ + Cl2 == 2Fe3+ + 2Cl-
(4)4FeS2(S) + 11O2(g) == 2Fe2O3(S) + 8SO2(g) ΔH = - 3408kl/mol
解析:
略

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目

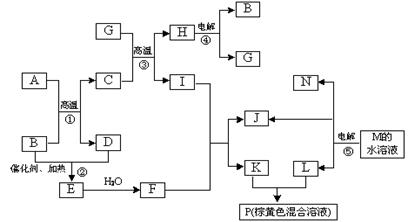
 的热化学方程式为:
的热化学方程式为: