题目内容
5.由环己烷可制备1,4-环已二醇的二醋酸酯.下图所示是有关的8步反应(其中所有无机产物都已略去):
回答下列问题:
(1)其中有3步属于取代反应、2步属于消去反应、3步属于加成反应.反应①和⑥、⑦属于取代反应.(填序号)
(2)化合物的结构简式是:B
 、C
、C .反应④所用试剂和条件是氢氧化钠醇溶液、加热.
.反应④所用试剂和条件是氢氧化钠醇溶液、加热.(3)写出第②步反应的化学方程式:
 .
.
分析 环己烷和氯气发生取代反应生成 ,
, 在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为:
在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为: ,A和氯气反应生成B,B发生消去反应生成
,A和氯气反应生成B,B发生消去反应生成 ,所以B的结构简式为
,所以B的结构简式为 ,则A和氯气发生加成反应生成B,
,则A和氯气发生加成反应生成B, 和溴发生1,4-加成反应生成
和溴发生1,4-加成反应生成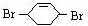 ,
,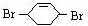 在氢氧化钠的水溶液、加热条件下发生取代反应生成C为
在氢氧化钠的水溶液、加热条件下发生取代反应生成C为 ,
, 与醋酸酐发生酯化反应生成D为
与醋酸酐发生酯化反应生成D为 ,D与氢气发生加成反应生成
,D与氢气发生加成反应生成 .
.
解答 解:环己烷和氯气发生取代反应生成 ,
, 在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为:
在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为: ,A和氯气反应生成B,B发生消去反应生成
,A和氯气反应生成B,B发生消去反应生成 ,所以B的结构简式为
,所以B的结构简式为 ,则A和氯气发生加成反应生成B,
,则A和氯气发生加成反应生成B, 和溴发生1,4-加成反应生成
和溴发生1,4-加成反应生成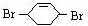 ,
,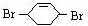 在氢氧化钠的水溶液、加热条件下发生取代反应生成C为
在氢氧化钠的水溶液、加热条件下发生取代反应生成C为 ,
, 与醋酸酐发生酯化反应生成D为
与醋酸酐发生酯化反应生成D为 ,D与氢气发生加成反应生成
,D与氢气发生加成反应生成 .
.
(1))根据上面的分析可知,反应①、⑥、⑦属于取代反应,
故答案为:⑥、⑦;
(2)B的结构简式为 ,C的结构简式为:
,C的结构简式为: ,反应④发生卤代烃的消去反应,所用试剂和条件是:氢氧化钠醇溶液、加热,
,反应④发生卤代烃的消去反应,所用试剂和条件是:氢氧化钠醇溶液、加热,
故答案为: ;
; ;氢氧化钠醇溶液、加热;
;氢氧化钠醇溶液、加热;
(3)反应②的反应方程式为: ,
,
故答案为: .
.
点评 本题考查有机物的合成,根据有机物的结构进行推断,熟练掌握官能团的性质与转化,试题培养了学生的分析、理解能力及逻辑推理能力.

练习册系列答案
相关题目
11.下列反应是氧化还原反应的是( )
| A. | NaOH+HCl═NaCl+H2O | B. | CuO+H2SO4═CuSO4+H2O | ||
| C. | Zn+2H+═Zn2++H2↑ | D. | CaO+H2O═Ca(OH)2 |
16.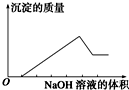 某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO3-、⑥Cl-、⑦OH-.向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )
某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO3-、⑥Cl-、⑦OH-.向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )
 某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO3-、⑥Cl-、⑦OH-.向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )
某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO3-、⑥Cl-、⑦OH-.向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )| A. | ①②⑤ | B. | ①③④ | C. | ②⑥⑦ | D. | ①②④⑥ |
10.国际无机化学命名委员会将长式元素周期表原先的主.副族号取消,从左往右改为18列,碱金属为第1列,稀有气体为18列.按这个规定,下列说法不正确的是( )
| A. | 第17.18列元素都是非金属元素 | |
| B. | 第14列元素形成的化合物种类最多 | |
| C. | 第3列元素种类最多 | |
| D. | 只有第2列元素的原子最外层有2个电子 |
17.结晶氯化铝(AlCl3•6H20)在精密铸造中可以代替氯化铵,也是生产净水剂聚合氯化铝的中间产品.以煤矸石(含有Al203、Fe203及Si02等)为原料制备结晶氯化铝是煤矸石资源利用的重要方式之一,工艺流程如下.请回答:
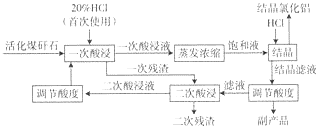
(1)结晶滤液的主要成分是AlCl3、FeCl3和HCl,二次残渣的主要成分是SiO2(填化学式).
(2)该工艺流程中可以循环使用的物质是盐酸,循环利用该物质的优点是充分利用原料降低成本,缺点是杂质的富集可能会影响后续AlCl3•6H2O产品的纯度.
(3)为了分析二次残渣中铁元素的含量,某同学称取5.000g二次残渣,先将其预处理使铁元素还原为Fe2+,并在容量瓶中配制成100mL溶液,然后移取25.00mL用1.000×l0-2mol•L-lKMn04标准溶液滴定,消耗标准溶液20.00mL.已知反应式为:Fe2++Mn04-+H+→Fe3++Mn2++H20(未配平),二次残渣中铁元素的质量分数为4.480%.
(4)下表为HCl通入体积对AlCl3结晶效率和HC1利用率的影响.
结晶效率变化的原因是氯化铝的溶解度会随着溶液中盐酸浓度的增加而下降;随HC1体积的增大,HC1利用率降低的原因可能是通入的HCl气体使溶液中的盐酸浓度升高,继续通入HCl气体,降低了气体在溶液中的吸收效率.
(5)将结晶氯化铝加入一定量蒸馏水,在lOO℃水浴中加热蒸干即可得到聚合氯化铝[Al2(OH)nCl6-n•H20]m.由结晶氯化铝制取Al2(OH)nCl6-n的化学方程式为2AlCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$Al2(OH)nCl6-n+nHCl+(12-n)H2O.

(1)结晶滤液的主要成分是AlCl3、FeCl3和HCl,二次残渣的主要成分是SiO2(填化学式).
(2)该工艺流程中可以循环使用的物质是盐酸,循环利用该物质的优点是充分利用原料降低成本,缺点是杂质的富集可能会影响后续AlCl3•6H2O产品的纯度.
(3)为了分析二次残渣中铁元素的含量,某同学称取5.000g二次残渣,先将其预处理使铁元素还原为Fe2+,并在容量瓶中配制成100mL溶液,然后移取25.00mL用1.000×l0-2mol•L-lKMn04标准溶液滴定,消耗标准溶液20.00mL.已知反应式为:Fe2++Mn04-+H+→Fe3++Mn2++H20(未配平),二次残渣中铁元素的质量分数为4.480%.
(4)下表为HCl通入体积对AlCl3结晶效率和HC1利用率的影响.
| HCl气体体积/(m3.L-1) | 结晶效率/% | HCl利用效率/% |
| 0.0375 | 11.8 | 93.2 |
| 0.075 | 31.5 | 89.8 |
| 0.1225 | 59.0 | 83.2 |
| 0.15 | 68.0 | 74.9 |
| 0.1875 | 71.0 | 67.8 |
| 0.225 | 73.1 | 59.1 |
(5)将结晶氯化铝加入一定量蒸馏水,在lOO℃水浴中加热蒸干即可得到聚合氯化铝[Al2(OH)nCl6-n•H20]m.由结晶氯化铝制取Al2(OH)nCl6-n的化学方程式为2AlCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$Al2(OH)nCl6-n+nHCl+(12-n)H2O.
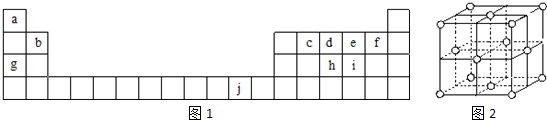
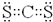 ,ci2与ce2比较,沸点较高的是CS2(写分子式).
,ci2与ce2比较,沸点较高的是CS2(写分子式).