题目内容
已知A是应用最为广泛的金属,X,Y为短周期同一主族的元素的单质,B和C是两种黑色化合物.A.B.C与有关物质之间的相互转化关系如图所示,其中每一方格内的字母表示一种反应物或生成物,反应加入或生成的水已略去.
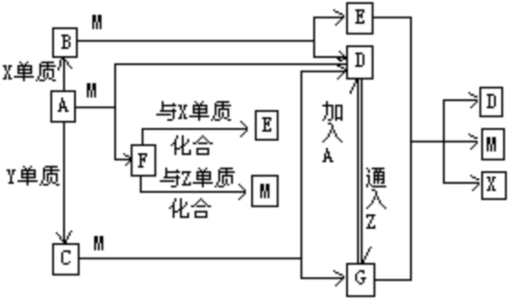
填写下列空白:
(1)物质的化学式:A ,B ,C .
(2)写出反应的化学方程式:
B+M:
C+M:
(3)写出E与G反应的离子方程式: .

填写下列空白:
(1)物质的化学式:A
(2)写出反应的化学方程式:
B+M:
C+M:
(3)写出E与G反应的离子方程式:
考点:无机物的推断
专题:推断题
分析:A是应用最为广泛的金属,则A为Fe,X,Y为短周期同一主族的元素的单质,分别与Fe反应生成的B、C是两种黑色化合物,则X、Y分别为O2、S中的一种,则对应B、C分别Fe3O4、FeS中的一种,且A、B、C都与M反应,考虑M属于酸,由D与G之间的相互转化,可知G中Fe为高价态,酸M为非氧化性酸,Z具有强氧化性,且与酸具有相同的元素,可推知Z为Cl2,D为FeCl2、G为FeCl3,M为HCl,由转化关系可知X为S,Y为O2,B为FeS,C为Fe3O4,E为H2S,F为H2,氢气与硫反应生成硫化氢,氢气与氯气反应生成HCl,硫化氢与氯化铁溶液反应生成氯化亚铁、HCl与硫,符合题意,据此解答.
解答:
解:A是应用最为广泛的金属,则A为Fe,X,Y为短周期同一主族的元素的单质,分别与Fe反应生成的B、C是两种黑色化合物,则X、Y分别为O2、S中的一种,则对应B、C分别Fe3O4、FeS中的一种,且A、B、C都与M反应,考虑M属于酸,由D与G之间的相互转化,可知G中Fe为高价态,酸M为非氧化性酸,Z具有强氧化性,且与酸具有相同的元素,可推知Z为Cl2,D为FeCl2、G为FeCl3,M为HCl,由转化关系可知X为S,Y为O2,B为FeS,C为Fe3O4,E为H2S,F为H2,氢气与硫反应生成硫化氢,氢气与氯气反应生成HCl,硫化氢与氯化铁溶液反应生成氯化亚铁、HCl与硫,符合题意,
(1)由上述分析可知,A为Fe,B为FeS,C为Fe3O4,故答案为:Fe;FeS;Fe3O4;
(2)B+M的反应生成氯化亚铁与盐酸反应生成氯化亚铁与硫化氢,化学反应方程式为:FeS+2HCl=FeCl2+H2S↑,
C+M的反应是四氧化三铁与盐酸反应生成氯化亚铁、氯化铁与水,化学反应方程式为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,
故答案为:FeS+2HCl=FeCl2+H2S↑;Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;
(3)E与G反应是硫化氢与氯化铁溶液反应生成氯化亚铁、HCl与硫,反应离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,
故答案为:2Fe3++H2S=2Fe2++S↓+2H+.
(1)由上述分析可知,A为Fe,B为FeS,C为Fe3O4,故答案为:Fe;FeS;Fe3O4;
(2)B+M的反应生成氯化亚铁与盐酸反应生成氯化亚铁与硫化氢,化学反应方程式为:FeS+2HCl=FeCl2+H2S↑,
C+M的反应是四氧化三铁与盐酸反应生成氯化亚铁、氯化铁与水,化学反应方程式为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,
故答案为:FeS+2HCl=FeCl2+H2S↑;Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;
(3)E与G反应是硫化氢与氯化铁溶液反应生成氯化亚铁、HCl与硫,反应离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,
故答案为:2Fe3++H2S=2Fe2++S↓+2H+.
点评:本题考查无机物推断,涉及Fe元素化合物性质与转化,综合分析转化关系确定M为酸是关键,需要学生熟练掌握元素化合物性质,对学生的逻辑推理有一定的要求,难度中等.

练习册系列答案
相关题目
往BaCl2溶液中通入SO2气体,溶液仍澄清;若将上述通入SO2气体的BaCl2溶液分盛于两支试管,一支加稀硝酸,另一支加烧碱溶液,结果两支试管都有白色沉淀.则下列结论合理的是( )
| A、氯化钡有两性 |
| B、两支试管中产生的沉淀均是亚硫酸钡 |
| C、SO2有还原性,其水溶液呈酸性 |
| D、增强碱性使SO2水溶液中SO32-浓度减小 |
生活中的下列现象,用分子的相关知识解释不正确的是( )
| A、水沸腾时能掀起壶盖,说明分子大小随温度升高而增大 |
| B、成熟的菠萝蜜会散发出浓浓的香味,说明分子在不断地运动 |
| C、湿衣服晾在太阳底下干得快,说明分子运动速率与温度有关 |
| D、液化石油气须加压后贮存在钢瓶中,说明分子之间有间隙 |
 (C)
(C)