题目内容
3.二氧化硅是酸性氧化物的原因是( )| A. | 它溶于水得到相应的酸 | B. | 它对应的水化物是可溶性强酸 | ||
| C. | 它与强碱反应只生成盐和水 | D. | 它是非金属氧化物 |
分析 酸性氧化物为:与碱反应生成盐和水的氧化物,或者与水反应生成对应酸,据此解答.
解答 解:A.二氧化硅不溶于水,与水不反应,故A错误;
B.二氧化硅对应的水化物是难溶性弱酸,故B错误;
C.二氧化硅和氢氧化钠反应生成硅酸钠和水,符合酸性氧化物的概念,故C正确;
D.非金属氧化物不一定是酸性氧化物,如NO、CO,故D错误;
故选:C.
点评 本题考查了酸性氧化物的判断,熟悉酸性氧化物的概念及二氧化硅的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
13.下面四种变化中,有一种变化与其他三种变化类型不同的是( )
| A. | CH3CH2OH+CH3COOH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O | |
| B. | CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O | |
| C. | 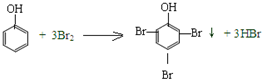 | |
| D. | CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O |
14.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| B. | 2.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.04NA | |
| C. | 7.8g Na2S和Na2O2的固体混合物中含有的阴离子数等于0.1NA | |
| D. | 常温下,5.6 g 铁钉与足量浓硝酸反应,转移的电子数为0.3 NA |
8.关于氯水的叙述不正确的是( )
| A. | 氯气和液氯是两种不同物质 | |
| B. | 新制氯水溶液中存在两个平衡状态 | |
| C. | 久置的氯水,溶液的PH会变小 | |
| D. | 向氯水中滴加紫色石蕊试剂,溶液先变红后褪色 |
15.下列化学反应,能用离子方程式H++OH-═H2O来表示的是( )
| A. | 盐酸和氢氧化铜 | B. | 硫酸和氢氧化钠溶液 | ||
| C. | 醋酸和氢氧化钡溶液 | D. | 稀硝酸和氨水混合 |
12.点燃一根蜡烛,用冷碟底放在蜡烛火焰上方,过一会儿,在碟底收集到炭黑,由此能得出石蜡的组成中一定含有( )
| A. | 碳元素 | B. | 氢元素 | C. | 氧元素 | D. | 氢、氧元素 |