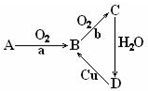
题目内容
9.下列物质间的转化在给定条件下能一步实现的是( )①NH3 $→_{催化剂/△}^{O_{2}}$NO2 $\stackrel{H_{2}O}{→}$HNO3
②SiO2 $\stackrel{NaOH}{→}$Na2SiO3$\stackrel{HCl}{→}$H2SiO3
③Mg(OH)2$\stackrel{HCl}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg
④Na$→_{△}^{O_{2}}$Na2O2$\stackrel{CO_{2}}{→}$Na2CO3
⑤FeS2$\stackrel{煅烧}{→}$SO3$\stackrel{水}{→}$H2SO4.
| A. | ①④⑤ | B. | ③④⑤ | C. | ②④ | D. | ①②③ |
分析 ①氨气催化氧化生成一氧化氮,一氧化氮被空气中氧气氧化为二氧化氮,二氧化氮溶于水生成硝酸;
②二氧化硅和氢氧化钠溶液反应生成硅酸钠和水,硅酸钠和盐酸反应生成硅酸沉淀;
③氢氧化镁溶解于盐酸生成氯化镁溶液,电解氯化镁溶液生成氢氧化镁、氯气和氢气;
④钠和氧气点燃反应生成过氧化钠,过氧化钠和二氧化碳反应生成碳酸钠;
⑤FeS2 高温煅烧生成二氧化硫,二氧化硫催化氧化生成三氧化硫,三氧化硫溶于水生成硫酸.
解答 解:①氨气催化氧化生成一氧化氮,4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,一氧化氮被空气中氧气氧化为二氧化氮,2NO+O2=2NO2,二氧化氮溶于水生成硝酸,氨气催化氧化不能一步生成二氧化氮,故①错误;
②二氧化硅和氢氧化钠溶液反应生成硅酸钠和水,SiO2+2NaOH=Na2SiO3+H2O,硅酸钠和盐酸反应生成硅酸沉淀Na2SiO3+2HCl=2NaCl+H2SiO3↓,各步能一步实现,故②正确;
③氢氧化镁溶解于盐酸生成氯化镁溶液,电解氯化镁溶液生成氢氧化镁、氯气和氢气,电解熔融氯化镁得到金属镁,氯化镁溶液不能一步反应生成金属镁,故③错误;
④钠和氧气点燃反应生成过氧化钠,2Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2,过氧化钠和二氧化碳反应生成碳酸钠2Na2O2+2CO2=2Na2CO3+O2,各步能一步实现,故④正确;
⑤FeS2 高温煅烧生成二氧化硫,二氧化硫催化氧化生成三氧化硫,三氧化硫溶于水生成硫酸,二硫化亚铁煅烧不能一步反应生成三氧化硫,故⑤错误;
故选C.
点评 本题考查了物质性质的应用,转化关系的分析判断,掌握物质性质是解题关键,题目难度中等.

练习册系列答案
相关题目
20.下列试剂的保存方法正确的是( )
| A. | 少量金属钠保存在乙醇中 | |
| B. | 新制氯水存放在带玻璃塞的无色细口瓶中 | |
| C. | 氢氧化钠固体保存在带橡胶塞的广口瓶中 | |
| D. | 浓硝酸保存在带橡胶塞的无色玻璃瓶中 |
17.某溶液中含有大量的下列离子:Fe3+、SO42-、Al3+和M离子,经测定Fe3+、SO42-、Al3+和M离子的物质的量之比为1:4:1:2,则M离子可能是下列中的( )
| A. | Na+ | B. | OH- | C. | S2- | D. | Ag+ |
4.下列有关物质性质或应用的说法正确的是( )
| A. | 制水泥和玻璃都用石灰石作原料 | |
| B. | 利用Al2O3制作的坩埚,可用于熔融烧碱 | |
| C. | Si可用作太阳能电池和光导纤维的材料 | |
| D. | 铜的金属活泼性比铁的弱,铜不能与任何强酸发生反应 |
14.北京提出2008年“绿色奥运”的口号,为改善北京空气质量,将冬季燃烧煤取暖改用天然气做燃料.主要是为了( )
| A. | 减少氮氧化物的排放 | B. | 降低对臭氧层的破坏 | ||
| C. | 减少二氧化碳的排放 | D. | 防止温室效应 |
1.常温时,等体积等物质的量浓度的下列物质的溶液中,其中正确的是( )
| A. | 溶液的pH:Na2CO3>NaHCO3>CH3COOH>NaHSO4 | |
| B. | 由水电离出的c(H+):Na2CO3>NaHCO3>NaHSO4>CH3COOH | |
| C. | 溶液中的c(NH4+):(NH4)2SO4>(NH4)2CO3>NH4HSO4>NH4Cl | |
| D. | 溶液的pH:(NH4)2CO3>(NH4)2SO4>NH4Cl>NH4HSO4 |
18.某气体在标准状况下的密度为1.696g•L-1,则该气体可能是( )
| A. | CO | B. | N2 | C. | CO2 | D. | F2 |
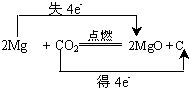
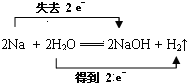 .
.