题目内容
(1)含有相同氧原子数的SO2和SO3其物质的量之比为 ,质量之比为 ,分子数之比为 ,硫原子数之比为 .
(2)在K2Cr2O7+14HCI═2KC1+3C12↑+7H2O+2CrCl3的反应中:
① 元素被氧化, 元素被还原, 是氧化剂.
②发生氧化反应的物质是 .
③在参加反应的盐酸中.起还原剂作用的HCl与起酸性作用的HCl的质量比为 .
④用双线桥标出该反应中电子转移的方向和数目 .
(2)在K2Cr2O7+14HCI═2KC1+3C12↑+7H2O+2CrCl3的反应中:
①
②发生氧化反应的物质是
③在参加反应的盐酸中.起还原剂作用的HCl与起酸性作用的HCl的质量比为
④用双线桥标出该反应中电子转移的方向和数目
考点:氧化还原反应的计算
专题:
分析:(1)结合SO2和SO3分子含有O原子数目计算二者的物质的量之比,根据m=nM计算二者质量之比,由N=nNA可知,分子数目之比等于物质的量之比,结合分子中含有S原子数目计算有二者含有硫原子数之比;
(2)①元素化合价升高,被氧化,元素化合价降低,被还有,所含元素化合价降低的反应物是氧化剂;
②所含元素化合价升高的反应物是还原剂,还原剂发生氧化反应;
③反应后氯元素化合价升高,HCl起还原作用,反应后Cl元素化合价不变,HCl起酸性作用;
④双线桥表示氧化还原反应,标“得或失”及电子数目,箭头表示反应前后变化,不表示电子转移方向.
(2)①元素化合价升高,被氧化,元素化合价降低,被还有,所含元素化合价降低的反应物是氧化剂;
②所含元素化合价升高的反应物是还原剂,还原剂发生氧化反应;
③反应后氯元素化合价升高,HCl起还原作用,反应后Cl元素化合价不变,HCl起酸性作用;
④双线桥表示氧化还原反应,标“得或失”及电子数目,箭头表示反应前后变化,不表示电子转移方向.
解答:
解:(1)SO2含有2个O原子,SO3分子含有3个O氧原子,故含有相同氧原子数的SO2和SO3的物质的量之比=
:
=3:2,二者质量之比=3×64:2×80=6:5,由N=nNA可知,分子数目之比等于物质的量之比=3:2,每个分子都含有1个S原子,故有二者含有硫原子数之比=3:2,
故答案为:3:2;6:5;3:2;3:2;
(2)①反应中Cl元素的化合价升高,被氧化,Cr元素的化合价降低,被还原,K2Cr2O7中铬元素的化合价降低,为氧化剂,
故答案为:Cl;Cr;K2Cr2O7;
②反应中HCl所含Cl元素的化合价升高,HCl做还原剂被氧化,发生氧化反应,故答案为:HCl;
③由方程式可以看出,14molHCl参加反应,有6mol被氧化生成氯气,另2molHCl生成KCl,6molHCl生成CrCl3,表现出酸性,起还原剂作用的HCl与起酸性作用的HCl的物质的量之比为6:8=3:4,
故答案为:3:4;
④反应中Cr元素化合价由+6价降低为+3价,Cl元素化合价由-1价升高为0价,转移电子数目总共为6,用双线桥表示电子转移情况是: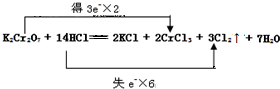 ,故答案为:
,故答案为: .
.
| 1 |
| 2 |
| 1 |
| 3 |
故答案为:3:2;6:5;3:2;3:2;
(2)①反应中Cl元素的化合价升高,被氧化,Cr元素的化合价降低,被还原,K2Cr2O7中铬元素的化合价降低,为氧化剂,
故答案为:Cl;Cr;K2Cr2O7;
②反应中HCl所含Cl元素的化合价升高,HCl做还原剂被氧化,发生氧化反应,故答案为:HCl;
③由方程式可以看出,14molHCl参加反应,有6mol被氧化生成氯气,另2molHCl生成KCl,6molHCl生成CrCl3,表现出酸性,起还原剂作用的HCl与起酸性作用的HCl的物质的量之比为6:8=3:4,
故答案为:3:4;
④反应中Cr元素化合价由+6价降低为+3价,Cl元素化合价由-1价升高为0价,转移电子数目总共为6,用双线桥表示电子转移情况是:
 ,故答案为:
,故答案为: .
.
点评:本题考查物质的量有关计算、氧化还原反应等,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念及电子转移表示,题目难度中等.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、石灰乳与氯气制漂白粉:2OH-+Cl2=ClO-+Cl-+H2O |
| B、铁与稀硫酸制氢气:Fe+6H+=2Fe3++3H2↑ |
| C、Ba(OH)2溶液中滴加过量NaHCO3溶液:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O |
| D、向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O=H2SiO3(胶体)+CO32- |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、通常情况下,22.4L乙烯中C-H键数为4NA |
| B、1mol羟基中电子数为10NA |
| C、在反应KIO3+6HI═KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
| D、常温下,1L 0.1mol?L-1的NH4NO3溶液中氮原子数为0.2NA |

