题目内容
14.表是不同温度下水的离子积数据:| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | α | 1×10-12 |
①若25<t1<t2,则α>1×10-14(填“>”“<”或“=”)
②25℃下,某Na2SO4溶液中c(SO42-)=1.0×10-4 mol•L-1,取该溶液1mL,加水稀释至10mL,则稀释后溶液中c (Na+):c (OH-)=1000:1
③t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=6,则V1:V2=1:1.此溶液中各种离子的浓度由大到小的排列顺序是c(Na+)=2c(SO42-)>c(H+)=c(OH-).
分析 ①水的电离是吸热反应,升高温度促进水电离,导致水的离子积常数增大;
②硫酸钠溶液是显中性的;
③混合液的pH=6,溶液呈中性,计算V1:V2,根据反应后溶液的组成分析各种离子的浓度大小.
解答 解:①水的电离为吸热反应,升高温度,平衡向着正反应方向移动,导致水的离子积常数增大,根据表格知,温度大小顺序是,25<t1<t2,则a>1×10-14,
故答案为:>;
②25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,则溶液中钠离子浓度是1×10-3 mol/L.如果稀释10倍,则钠离子浓度是1×10-4 mol/L.但硫酸钠溶液是显中性的,所以c(Na+):c(OH-)=10-4:10-7=1000:1,
故答案为:1000:1;
③t2℃时,将pH=11的苛性钠中氢氧根离子浓度为:c(OH-)=$\frac{1×1{0}^{-12}}{1×1{0}^{-11}}$mol/L=0.1mol/L,
pH=1的稀硫酸中氢离子浓度为0.1mol/L,
pH=2的溶液中氢离子浓度为0.01mol/L,
则混合液中满足:0.1mol/L×V2=0.1mol/L×V1,整理可得:V1:V2=1:1,故溶液中各种离子的浓度由大到小的排列顺序是:c(Na+)+c(H+)=2c(SO42-)+c(OH-),而混合溶液的pH=6,所以c c ccc(H+)=c(OH-),
故答案为:1:1;c(Na+)=2c(SO42-)>c(H+)=c(OH-).
点评 本题考查了水的电离、溶液中离子浓度大小比较以及pH计算,题目难度中等,该题是高考中的常见题型,属于中等难度的试题;该题的关键是明确溶液中几个重要守恒关系,即电荷守恒、物料守恒和质子守恒.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列实验装置不能达到实验目的是( )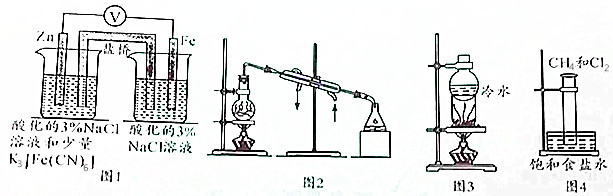

| A. | 用图1所示装置验证牺牲阳极的阴极保护法 | |
| B. | 用图2所示装置可在实验室制备蒸馏水 | |
| C. | 用图3所示装置可以进行NaCl与NH4Cl、NaCl与I2的分离 | |
| D. | 用图4所示装置进行CH4取代反应的实验 |
9.有机物 ①CH2OH(CHOH)4CHO,②CH3CH2CH2OH,③CH2═CH-CH2OH,④CH2═CH-COOCH3,⑤CH2═CH-COOH中,既能发生加成反应、酯化反应,又能发生氧化反应的是( )
| A. | ③⑤ | B. | ②④ | C. | ①③⑤ | D. | ①③ |
19.表是元素周期表的一部分,表中序号分别代表某一元素.请回答下列问题.
(1)①-⑩中,最活泼的金属元素是Na(写元素符号,下同);最不活泼的元素是Ar;可作半导体材料的元素是Si;某元素的气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐,该元素是N.
(2)④、⑤的简单离子,其半径更大的是F-(写离子符号).
(3)⑧、⑨的气态氢化物,更稳定的是HCl(填化学式).
(4)③的最低价气态氢化物分子中的化学键类型为极性键(填“极性键”或“非极性键”),该分子的空间构型为为V形,③的最低价气态氢化物比⑧的最低价气态氢化物沸点高(填“高”或“低”),原因是H2O分子之间含氢键
(5)元素的非金属性:①> ⑦(填“>”或“<”).
(6)①-⑨的最高价氧化物的水化物中:酸性最强的是HClO4(填化学式);碱性最强的是NaOH(填化学式),它与⑨的最高价氧化物的水化物反应的化学方程式为NaOH+HClO4=NaClO4+H2O.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)④、⑤的简单离子,其半径更大的是F-(写离子符号).
(3)⑧、⑨的气态氢化物,更稳定的是HCl(填化学式).
(4)③的最低价气态氢化物分子中的化学键类型为极性键(填“极性键”或“非极性键”),该分子的空间构型为为V形,③的最低价气态氢化物比⑧的最低价气态氢化物沸点高(填“高”或“低”),原因是H2O分子之间含氢键
(5)元素的非金属性:①> ⑦(填“>”或“<”).
(6)①-⑨的最高价氧化物的水化物中:酸性最强的是HClO4(填化学式);碱性最强的是NaOH(填化学式),它与⑨的最高价氧化物的水化物反应的化学方程式为NaOH+HClO4=NaClO4+H2O.
6.共价键、离子键和分子间作用力是物质间的不同作用力,下述物质中只含上述一种作用力的是( )
| A. | 冰 | B. | 过氧化钠 | C. | 氯化钠 | D. | 白磷 |
3.下列叙述正确的是( )
| A. | 1H和2H是不同的核素,它们的中子数相同 | |
| B. | 6Li和7Li的质子数相等,电子数也相等 | |
| C. | 14C和14N的质子数不等,它们的中子数相等 | |
| D. | 13C和14C属于同一种元素,它们的质量数相等 |
4.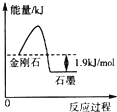 根据表中的信息判断下列说法错误的是( )
根据表中的信息判断下列说法错误的是( )
 根据表中的信息判断下列说法错误的是( )
根据表中的信息判断下列说法错误的是( )| 物质 | 外观 | 燃烧热/(kJ•mol-1) |
| 金刚石 | 无色、透明固体 | 395.4 |
| 石墨 | 灰黑,不透明固体 | 393.5 |
| A. | 由表中信息可得如图所示的图象 | |
| B. | 由表中信息知C(石墨,s)=C(金刚石,s)△H=+1.9 kJ•mol-1 | |
| C. | 由表中信息可知相同条件下金刚石的熔点低于石墨的熔点 | |
| D. | 石墨燃烧热的热化学方程式为C(石墨,s)+$\frac{1}{2}$O2(g)═CO(g)△H=-393.5 kJ•mol-1 |
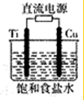 铜是人类最早利用的金属之一,铜能形成多种重要的化合物.
铜是人类最早利用的金属之一,铜能形成多种重要的化合物.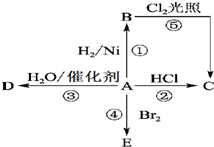 某气态烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A也是一种植物生长调节剂,A可发生如图所示的一系列化学反应.根据该图回答下列问题:
某气态烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A也是一种植物生长调节剂,A可发生如图所示的一系列化学反应.根据该图回答下列问题: