题目内容
19.在指定环境中可能大量共存的离子组是( )| A. | 强碱性的溶液中,Na+、S2-、[Al(OH)4]-、SO32- | |
| B. | 酸性溶液中,Fe2+、Na+、NO3-、SO42- | |
| C. | 能与铝放出H2的溶液中、K+、Cu2+、NO3-、SO42- | |
| D. | 无色溶液中Ca2+、Cu2+、ClO-、NO3- |
分析 A.碱性条件下离子之间不发生任何反应;
B.酸性条件下离子发生氧化还原反应;
C.能与铝放出H2的溶液可能为强碱性或非氧化性酸溶液;
D.有颜色的离子不能存在.
解答 解:A.碱性条件下离子之间不发生任何反应,可大量共存,故A正确;
B.酸性条件下Fe2+、NO3-离子发生氧化还原反应,不能大量共存,故B错误;
C.能与铝放出H2的溶液可能为强碱性或非氧化性酸溶液,碱性条件下Cu2+不能大量存在,酸性条件下不能存在NO3-离子,否则不能生成氢气,故C错误;
D.Cu2+有颜色,不能存在,故D错误.
故选A.
点评 本题考查离子共存问题,为高频考点,侧重于学生的分析能力的考查,难度不大,本题注意把握题中各项要求,为解答该题的关键,学习中注意把握相关离子的性质.

练习册系列答案
相关题目
10.向21.6g Fe3O4、Fe2O3、FeO、Cu的混合物中加入0.5mol•L-1的硫酸溶液420mL时,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
| A. | 1.12 g | B. | 2.24 g | C. | 3.36 g | D. | 6.40 g |
9.在一定条件下,2N02?N204正反应放热,达到平衡,下列说法正确的是( )
| A. | 在密闭定容体系中降温,混合气颜色变浅,体系压强增大 | |
| B. | 只降温,混合气体颜色变浅,说明正反应是放热的 | |
| C. | 加压时,混合气颜色开始变浅,后来又逐渐加深 | |
| D. | 加压时,混合气颜色开始变深,后来又逐渐变浅 |
 Al(OH)3
Al(OH)3 AlO2-+H++H2O,加入NaOH溶液,H+被中和,浓度减低,Al(OH)3不断溶解.
AlO2-+H++H2O,加入NaOH溶液,H+被中和,浓度减低,Al(OH)3不断溶解.
 请回答:
请回答: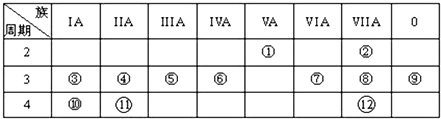
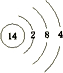 ,写出①的气态氢化物分子的电子式
,写出①的气态氢化物分子的电子式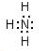 .
.