题目内容
充满HCl的烧瓶做完喷泉实验后得到的稀盐酸,用标准碳酸钠溶液滴定这种盐酸测定它的准确浓度,请你回答下列问题:
(1)用标准Na2CO3溶液滴定这种盐酸时,Na2CO3溶液应装在 式滴定管中,若用甲基橙作指示剂,达到滴定终点时,溶液从 色变为 色.
(2)现配制三种浓度的标准Na2CO3溶液,你认为最合适的是下列第 种.
①2.500mol?L-1 ②0.25mol?L-1③0.025mol?L-1
(3)若采用上述合适浓度的标准Na2CO3溶液滴定,用c(Na2CO3)表示,滴定时实验数据列表如下:
求这种待测稀盐酸的物质的量浓度(用数据和符号列式即可):c(HCl)= .
(1)用标准Na2CO3溶液滴定这种盐酸时,Na2CO3溶液应装在
(2)现配制三种浓度的标准Na2CO3溶液,你认为最合适的是下列第
①2.500mol?L-1 ②0.25mol?L-1③0.025mol?L-1
(3)若采用上述合适浓度的标准Na2CO3溶液滴定,用c(Na2CO3)表示,滴定时实验数据列表如下:
| 实验次数编号 | 待 待测盐酸体积(mL) | 滴入Na2CO3 溶液体积(mL) |
| 1 | 20.00 | 19.80 |
| 2 | 20.00 | 16.95 |
| 3 | 20.00 | 17.05 |
考点:中和滴定
专题:实验题
分析:(1)碳酸钠溶液呈碱性,用碱式滴定管盛装碳酸钠溶液;滴定终点时,溶液颜色由红色变为橙色且半分钟内不变色;
(2)为减小误差,应尽量用浓度小的溶液;
(3)舍去标准碳酸钠溶液滴定体积的不合理数据,求出碳酸钠溶液的平均体积,然后根据2HCl~Na2CO3求稀盐酸的物质的量浓度.
(2)为减小误差,应尽量用浓度小的溶液;
(3)舍去标准碳酸钠溶液滴定体积的不合理数据,求出碳酸钠溶液的平均体积,然后根据2HCl~Na2CO3求稀盐酸的物质的量浓度.
解答:
解:(1)碳酸钠溶液呈碱性,用碱式滴定管盛装碳酸钠溶液;滴定终点时,溶液颜色由红色变为橙色且半分钟内不变色,故答案为:碱;红;橙;
(2)实验时,为减小实验误差,则所用碳酸钠溶液体积不能过小,否则误差较大,应用浓度最小的,故答案为:③;
(3)舍去第一组数据,碳酸钠溶液的平均体积为
mL,
2HCl~~~~~~~Na2CO3
2 1
c(HCl)×20.00mL 0.025mol/L×
mL
C(HCl)=
×
mol×L-1=
mol/L,
故答案为:
mol/L.
(2)实验时,为减小实验误差,则所用碳酸钠溶液体积不能过小,否则误差较大,应用浓度最小的,故答案为:③;
(3)舍去第一组数据,碳酸钠溶液的平均体积为
| 16.95+17.05 |
| 2 |
2HCl~~~~~~~Na2CO3
2 1
c(HCl)×20.00mL 0.025mol/L×
| 16.95+17.05 |
| 2 |
C(HCl)=
| 2×C(Na2CO3) |
| 20.00 |
| (16.95+17.05) |
| 2 |
| 34c(Na2CO3) |
| 20.00 |
故答案为:
| 34c(Na2CO3) |
| 20.00 |
点评:本题考查中和滴定操作、计算,为高频考点,侧重于学生的分析、计算和实验能力的考查,注意把握中和滴定的操作原理和实验方法,难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
t°C时,某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下该反应的平衡常数表达为K=
,有关该平衡体系的说法正确的是( )
| c(X)?c2(Y) |
| c2(Z)?c2(W) |
| A、升高温度,平衡常数K一定增大 |
| B、增大压强,W(g)质量分数增加 |
| C、该反应的化学反应方程式为X+2Y?2Z+2W |
| D、增大X(g)浓度,平衡向逆反应方向移动 |
按系统命名法, 无标题的正确的名称是( )
无标题的正确的名称是( )
 无标题的正确的名称是( )
无标题的正确的名称是( )| A、3,3-二甲基-4-乙基戊烷 |
| B、3,3-二甲基-2-乙基戊烷 |
| C、3,4,4-三甲基己烷 |
| D、3,3,4-三甲基己烷 |
以下物质不能由两种单质直接反应得到的是( )
| A、CO2 |
| B、FeCl3 |
| C、MgO |
| D、FeCl2 |
某温度下,向2L恒容密闭容器中充入1.0mol A和1.0mol B,反应A(g)+B(g)?C(g)经过一段时间后达到平衡.反应过程中测定的部分数据见下表,下列说法正确的是( )
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A、反应在前5 s的平均速率v(A)=0.17 mol?L-1?s-1 |
| B、保持其他条件不变,升高温度,平衡时c(A)=0.41 mol?L-1,则反应的△H>0 |
| C、相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的转化率大于80% |
| D、相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v(正)<v(逆) |
下列对合成材料的认识不正确的是( )
| A、苯酚和甲醛在一定条件下可合成酚醛树脂 |
B、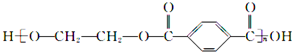 的单体是HOCH2CH2OH与 的单体是HOCH2CH2OH与 |
| C、聚苯乙烯是由苯乙烯加聚生成的纯净物 |
D、 的单体有3种 的单体有3种 |



 的部分流程图:
的部分流程图:
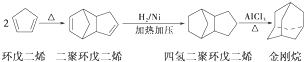
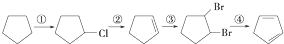
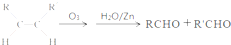 .请写出下列反应产物的结构简式:
.请写出下列反应产物的结构简式: