题目内容
电解稀H2SO4、Cu(NO3)2、NaCl的混合液,最初一段时间阴极和阳极上分别析出的物质分别是( )
| A、H2和Cl2 |
| B、Cu和Cl2 |
| C、H2和O2 |
| D、Cu和O2 |
考点:电解原理
专题:电化学专题
分析:电解原理是惰性电极通电条件下,溶液中阳离子移向阴极,阴离子移向阳极,依据溶液中阴离子放电顺序和阳离子的放电顺序分析判断生成产物,书写电极反应,根据电子守恒计算判断;
解答:
解:电解原理是惰性电极通电条件下,溶液中阳离子移向阴极,阴离子移向阳极,电解稀H2SO4、Cu(NO3)2、NaCl的混合液,阳离子放电顺序为Cu2+>H+>Na+,电极反应为:Cu2++2e-═Cu;阴离子放电顺序Cl->SO42-和NO3-,电极反应为:2Cl--2e-═Cl2↑,所以最初一段时间阴极和阳极上分别析出的物质分别是Cu和Cl2;
故选:B.
故选:B.
点评:本题考查了电解原理的分析判断,电极反应和电极产物的分析应用,溶液中离子放电顺序是解题关键,题目较简单.

练习册系列答案
相关题目
能正确表示下列反应的离子方程式是( )
| A、Ba(OH)2与MgSO4反应:Mg2++2OH-═Mg(OH)2↓ |
| B、铜片插入到硝酸银溶液中:Cu+Ag+═Cu2++Ag |
| C、硫酸铝溶液与氯化钡溶液混合:Ba2++SO42-═BaSO4↓ |
| D、碳酸钙溶于稀醋酸中:CaCO3+2H+═Ca2++H2O+CO2↑ |
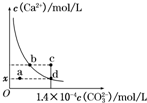 室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9 mol2/L2,下列说法不正确的是( )
室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9 mol2/L2,下列说法不正确的是( )| A、x数值为2×10-5 |
| B、c点时有碳酸钙沉淀生成 |
| C、加入蒸馏水可使溶液由d点变到a点 |
| D、b点与d点对应的溶度积相等 |
 按如图所示的装置进行实验:A极是铜锌合金,B极是纯铜,电解质溶液中含有足量的铜离子,通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03g,则A合金中Cu、Zn的物质的量之比为( )
按如图所示的装置进行实验:A极是铜锌合金,B极是纯铜,电解质溶液中含有足量的铜离子,通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03g,则A合金中Cu、Zn的物质的量之比为( )| A、4:1 | B、3:1 |
| C、2:1 | D、1:1 |
下列关于阿伏加德罗常数NA的说法正确的是( )
| A、1mol/L的NaCl溶液中Na+为NA个 |
| B、1mol水中H原子为2NA个 |
| C、1mol N2H4分子中N和H原子都为NA个 |
| D、2g H2中含NA个电子 |
在一定温度和压强下,2mol A2气体与3mol B2气体化合生成2mol气体化合物,则该化合物的化学式为( )
| A、AB3 |
| B、AB |
| C、A3B |
| D、A2B3 |
人们在研究金星大气成分时发现金星大气中有一种称为硫化羰(COS)的分子,其结构与CO2类似,硫化羰是一种与生命密切相关的物质,下列有关COS的推测不正确的是( )
| A、COS的熔点高于CO2 |
B、COS的电子式为: |
| C、COS的分子中所有原子满足8电子稳定结构 |
| D、硫化羰分子中三个原子处于同一直线上 |
