题目内容
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=5.6×10-5,求此温度下该反应CaSO4(s)+CO32-?CaCO3(s)+SO42-的平衡常数K的数值为 .
考点:难溶电解质的溶解平衡及沉淀转化的本质,化学平衡常数的含义
专题:
分析:以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq)平衡常数概念写出计算式,依据硫酸钙、碳酸钙溶度积常数的计算表达式,转化关系中钙离子相同计算分析.
解答:
解:溶浸过程中会发生:CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq),CaCO3(s)=Ca2++CO32-;CaSO4(s)=Ca2++SO42-,由硫酸钙、碳酸钙溶度积常数的计算表达式可知该反应的平衡常数K=
=
=
=1.75×104,
故答案为:1.75×104.
| [SO42-] |
| [CO32-] |
| Ksp(CaSO4) |
| Ksp(CaCO3) |
| 4.90×10-5 |
| 2.80×10-9 |
故答案为:1.75×104.
点评:本题考查了溶度积常数在计算中的应用等,侧重于基础知识的综合应用的考查,题目难度中等.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
在①乙炔、②乙烯、③苯、④甲苯四种有机化合物中,所有原子均在同一平面的是( )
| A、①②④ | B、①②③ |
| C、③④ | D、②③④ |
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
| A、异戊二烯与等物质的量的溴发生加成反应 |
| B、邻羟基苯甲酸与小苏打溶液反应 |
| C、甲苯在一定条件下发生硝化反应生成一硝基甲苯的反应 |
| D、2-氯丁烷[CH3CH(Cl)CH2CH3]与氢氧化钠乙醇溶液共热消去HCl分子的反应 |
室温,把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液以等体积混合,则混合液中微粒浓度关系正确的为( )
| A、c (CH3COO-)>c (Na+) |
| B、c (OH-)>c (H+) |
| C、c (CH3COOH)>c (CH3COO-) |
| D、c (CH3COOH)+c (CH3COO-)=0.02mol/L |
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A、原子半径:Y>Z>W |
| B、非金属性最强的元素为W |
| C、Y的最高价氧化物的熔点较高 |
| D、XW2分子中各原子最外层电子均达到8电子结构 |
下列物质中分子内和分子间均可形成氢键的是( )
| A、NH3 |
B、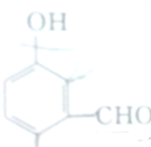 |
| C、H2S |
| D、C2H5OH |
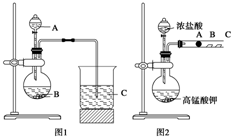 某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律.A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸.(已知高锰酸钾与浓盐酸反应生成氯气)
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律.A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸.(已知高锰酸钾与浓盐酸反应生成氯气)