题目内容
大气中的部分碘源于O3对海水中I-的氧化。将O3持续通入NaI溶液中进行模拟研究。
(1)在溶液中存在化学平衡:I2(aq)+I-(aq)
 (aq),其平衡常数表达式为________。
(aq),其平衡常数表达式为________。
(2)为探究Fe2+对O3氧化I-反应的影响(反应体系如图1),某研究小组测定两组实验中 浓度和体系pH,结果见图2和下表。
浓度和体系pH,结果见图2和下表。
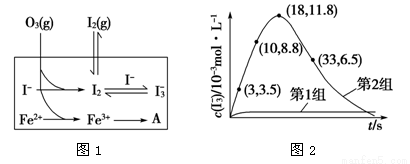

①第1组实验中,导致反应后pH升高的原因是______________________________。
②图1中的A为________。由Fe3+生成A的过程能显著提高I-的转化率,原因是_________。
③第2组实验进行18 s后, 浓度下降。导致下降的直接原因有________。
浓度下降。导致下降的直接原因有________。
A.c(H+)减小 B.c(I-)减小 C.I2(g)不断生成 D.c(Fe3+)增加
(3)据图2,计算3~18 s内第2组实验中生成 的平均反应速率(写出计算过程,结果保留两位有效数字)。
的平均反应速率(写出计算过程,结果保留两位有效数字)。
26.(1)  (2)①反应中H+被消耗,生成水。 ②Fe2+ ,Fe3+ 能氧化I—,提高其转化速率。③B.D (3) 5.5×10-4 mol/(L.s)
(2)①反应中H+被消耗,生成水。 ②Fe2+ ,Fe3+ 能氧化I—,提高其转化速率。③B.D (3) 5.5×10-4 mol/(L.s)
【解析】
试题分析:依据平衡常数的定义I2(aq) + Iˉ(aq)  I3ˉ(aq)的平衡常数表达式为:
I3ˉ(aq)的平衡常数表达式为: 。
。
(2)①该反应消耗H+,随反应进行c(H+)浓度降低,pH升高,方程式为:2I-(aq)+O3(g)+2H+(aq)=I2(aq)+O2(g)+H2O(l);②根据2Fe3++2Ⅰ-=Ⅰ2+2Fe2+,使平衡向c(I-)减小的方向移动,显著提高Ⅰ-的转化率,可知A为Fe2+,答案为:Fe2+;Fe3+ 能氧化I—,提高其转化速率。③c(Fe3+)增加,发生反应:2Fe3++2Ⅰ-=Ⅰ2+2Fe2+,c(I-)减小平衡逆向移动;故c(Fe3+)增加,c(I-)减小都会使c(I3-)急剧减小,答案为:BD;
(3)3~18s内,v(I3-)=(11.8X10-3-3.5X10-3)/15=5.5×10-4mol/(L?S),答案为:5.5×10-4mol/(L?S).
考点:考查化学反应与能量、化学反应速率、化学平衡。

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) ΔH=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)??
FeO(s)+CO(g) ΔH=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)?? FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
温度(T) | K1 | K2 |
973 | 1.47 | 2.38 |
1 173 | 2.15 | 1.67 |
(1)从上表可推断,反应①是________(填“放”或“吸”)热反应。
(2)现有反应③H2(g)+CO2(g)? CO(g)+H2O(g) ΔH=Q的平衡常数为K3。
CO(g)+H2O(g) ΔH=Q的平衡常数为K3。
Ⅰ.根据反应①与②推导出K1、K2、K3的关系式K3=___ _____;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有________。
A.缩小容器体积 B.降低温度
C.使用合适的催化剂 D.设法减少CO的量
E.升高温度
Ⅱ.根据反应①与②推导出Q1、Q2、Q3的关系式Q3=________。
一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g),则下列说法正确的是
CH3OCH3(g)+H2O(g),则下列说法正确的是
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 |
|
|
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
A、该反应的正方应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行

 xC(g)的生成物 C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
xC(g)的生成物 C在反应混合物中的百分含量(C%)和反应时间(t)的关系。