题目内容
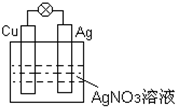 如右图所示
如右图所示(1)负极材料是
(2)正极的电极反应式为
(3)电池工作时总反应的离子方程式是
(4)电子的流向
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该电池中,Cu易失电子作负极、Ag作正极,负极反应式为Cu-2e+═Cu2+,正极反应式为Ag++e-═Ag,电子从负极沿导线流向正极.
解答:
解:(1)该原电池中,Cu的活泼性大于Ag,所以Cu易失电子作负极,Ag作正极,故答案为:Cu;
(2)正极上银离子得电子发生还原反应,电极反应式为Ag++e-═Ag,故答案为:Ag++e-═Ag;
(3)该原电池反应式与Cu和硝酸银发生置换反应相同,所以其电池离子反应式为Cu+2Ag+═2Ag+Cu2+,故答案为:Cu+2Ag+═2Ag+Cu2+;
(4)放电时,负极上失电子、正极上得电子,所以电子从负极Cu沿导线流向正极Ag,故答案为:铜到银(或负极到正极).
(2)正极上银离子得电子发生还原反应,电极反应式为Ag++e-═Ag,故答案为:Ag++e-═Ag;
(3)该原电池反应式与Cu和硝酸银发生置换反应相同,所以其电池离子反应式为Cu+2Ag+═2Ag+Cu2+,故答案为:Cu+2Ag+═2Ag+Cu2+;
(4)放电时,负极上失电子、正极上得电子,所以电子从负极Cu沿导线流向正极Ag,故答案为:铜到银(或负极到正极).
点评:本题考查了原电池原理,明确正负极判断、电极反应式的书写、电子流向即可解答,题目难度不大.

练习册系列答案
相关题目
下列说法或表示方法中正确的是( )
| A、等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B、氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ/mol |
| C、测定中和热的实验中,NaOH要稍过量,以使HCl完全中和 |
| D、Ba(OH)2?8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)△H<0 |
 过硫酸:
过硫酸:
 (b)
(b) (c)H2O2(d)
(c)H2O2(d) (e)
(e)
 (g)O3 (h)
(g)O3 (h)