题目内容
4.以下实验能获得成功的是( )| A. | 用溴水鉴别甲苯、己烷、己烯 | |
| B. | 将稀硫酸、稀硝酸和苯混合加热制硝基苯 | |
| C. | 苯和硝基苯混合物采用分液的方法分离 | |
| D. | 用CuSO4溶液除去由电石和水反应生成的乙炔气体中的杂质 |
分析 A.甲苯、己烷均与溴水反应,不溶于水,分层现象相同;
B.苯与浓硝酸、浓硫酸制备硝基苯;
C.苯和硝基苯互溶;
D.由电石和水反应生成的乙炔气体中混有硫化氢,硫化氢与硫酸铜反应,而乙炔不能.
解答 解:A.甲苯、己烷均与溴水反应,不溶于水,分层现象相同,不能鉴别,故A错误;
B.苯与浓硝酸、浓硫酸制备硝基苯,浓硫酸作催化剂、吸水剂,故B错误;
C.苯和硝基苯互溶,不能分液分离,应选蒸馏法,故C错误;
D.由电石和水反应生成的乙炔气体中混有硫化氢,硫化氢与硫酸铜反应,而乙炔不能,则利用硫酸铜溶液可除杂,故D正确;
故选D.
点评 本题考查化学实验方案的评价,涉及物质的鉴别和检验、混合物分离提纯,为高频考点,把握物质的性质、发生的反应和现象为解答的关键,侧重分析与应用能力的考查,注意有机物的性质及实验评价性分析,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
14.铝土矿是工业炼铝的主要原料,某铝土矿样品组成如下:
主要成分:Al2O3杂质:Fe2O3、SiO2及其他不溶且不参与化学反应的物质为测定该样品中Al的含量,某化学兴趣小组设计了如下两个方案:
【查阅资料】各相关离子开始沉淀和沉淀完全时溶液的pH如表:
方案一:将铝土矿加足量盐酸溶解,再调节pH,使Fe3+沉淀完全而Al3+不沉淀.需调节pH范围应是3.2~3.4,若想得到氯化铝固体需将其溶液通入HCl气流中直至蒸干.
方案二:

(1)②反应的离子方程式为OH-+CO2=CO32-+H2O,2AlO2-+CO2+3H2O=CO32-+2Al(OH)3↓.CO2不可过量的原因是防止SiO32-被沉淀.
(2)若在步骤②中加入乙酸乙酯调节pH,加热也可得到d的沉淀,写出生成d沉淀的化学方程式AlO2-+CH3COOCH2CH3+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CH3COO-+Al(OH)3↓+CH3CH2OH.
主要成分:Al2O3杂质:Fe2O3、SiO2及其他不溶且不参与化学反应的物质为测定该样品中Al的含量,某化学兴趣小组设计了如下两个方案:
【查阅资料】各相关离子开始沉淀和沉淀完全时溶液的pH如表:
| Al3+ | Fe3+ | AlO2- | SiO32- | |
| 开始沉淀时 | 3.4 | 1.9 | 10.6 | 7.3 |
| 沉淀完全时 | 4.7 | 3.2 | 9.3 | 5.3 |
方案二:

(1)②反应的离子方程式为OH-+CO2=CO32-+H2O,2AlO2-+CO2+3H2O=CO32-+2Al(OH)3↓.CO2不可过量的原因是防止SiO32-被沉淀.
(2)若在步骤②中加入乙酸乙酯调节pH,加热也可得到d的沉淀,写出生成d沉淀的化学方程式AlO2-+CH3COOCH2CH3+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CH3COO-+Al(OH)3↓+CH3CH2OH.
19.某链状有机物分子中含x个-CH3,y个-CH2-,z个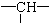 ,其余为氯原子.则氯原子的个数为( )
,其余为氯原子.则氯原子的个数为( )
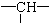 ,其余为氯原子.则氯原子的个数为( )
,其余为氯原子.则氯原子的个数为( )| A. | 2y+3x-x | B. | z+2-x | C. | 2y+z-x | D. | z+2y+2-x |
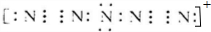 .
.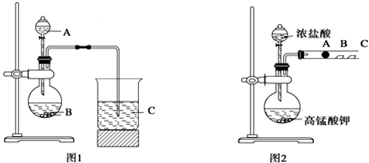
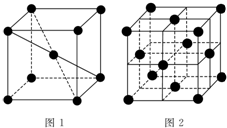 1 183K以下纯铁晶体的基本结构单元如图1所示,1 183K以上转变为图2所示结构的基本结构单元,在1中铁原子的配位数为8;其中为密堆积的是2(填“1”或“2”);1中的空间利用率为68%.
1 183K以下纯铁晶体的基本结构单元如图1所示,1 183K以上转变为图2所示结构的基本结构单元,在1中铁原子的配位数为8;其中为密堆积的是2(填“1”或“2”);1中的空间利用率为68%.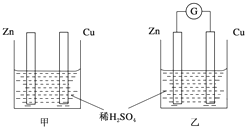 ①分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计.请回答下列问题:
①分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计.请回答下列问题: .
. .
.