题目内容
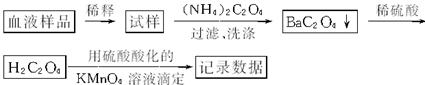
测定血液中Ca2+的含量,可将用蒸馏水稀释的血液与草酸铵溶液反应,使Ca2+全部变为草酸钙,将过滤的沉淀加入稀硫酸溶解,再用KMnO4溶液生成草酸,有关的化学反应如下:Ca2++C2O![]() ====CaC2O4↓ CaC2O4+H2SO4====CaSO4+H2C2O4
====CaC2O4↓ CaC2O4+H2SO4====CaSO4+H2C2O4
2KMnO4+5H2C2O4+3H2SO4====K2SO4+2MnSO4+10CO2↑+8H2O
现量取10.00 mL血样,用上述方法测定血钙含量时,耗用0.1200 mol·L-1 KMnO4溶液5.0 mL恰好达滴定终点,则此血样中的含钙量为( )
A.2.40 g·L-1 B.3.00 g·L-1
C.6.00 g·L-1 D.4.80 g·L-1
C
解析:Ca2+的含量为
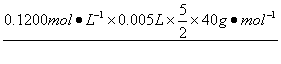 =6.00 g·L-1。
=6.00 g·L-1。

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目