题目内容
现有四种晶体,其离子排列方式如图所示,其中化学式正确的是( )
A、 AB2 AB2 |
B、 EF2 EF2 |
C、 XYZ3 XYZ3 |
D、 AB AB |
考点:晶胞的计算
专题:化学键与晶体结构
分析:根据微粒所在晶胞位置,利用均摊法计算微粒数目之比,得到化学式.
解答:
解:A.A位于体心,数目为1,B位于顶点,数目为8×
=1,微粒数目为1:1,即化学式为AB,故A错误;
B.E和F分别位于晶胞的顶点位置,各占4个,即晶胞中两种微粒数目相等,化学式为EF,故B错误;
C.X位于体心,数目为1,Y位于面心,数目为6×
=3,Z位于顶点,数目为8×
=1,微粒数目比值为1:3:1,化学式为XY3Z,故C错误;
D.A位于顶点和面心,数目为8×
+6×
=4,B位于棱心和体心,数目为12×
+1=4,数目之比为1:1,化学式为AB,故D正确;
故选D.
| 1 |
| 8 |
B.E和F分别位于晶胞的顶点位置,各占4个,即晶胞中两种微粒数目相等,化学式为EF,故B错误;
C.X位于体心,数目为1,Y位于面心,数目为6×
| 1 |
| 2 |
| 1 |
| 8 |
D.A位于顶点和面心,数目为8×
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
故选D.
点评:本题考查利用均摊法计算化学式,利用均摊法计算出微粒数目之比,从而得到化学式.

练习册系列答案
相关题目
下列各电子式中正确的是( )
A、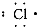 氯原子 |
B、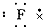 氟原子 |
C、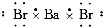 溴化钡 |
D、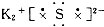 硫化钾 |
下列有关电池的叙述正确的是( )
| A、锌锰干电池工作一段时间后碳棒变细 |
| B、最早使用的充电电池是锌锰电池 |
| C、锂离子电池是新一代可充电的绿色电池 |
| D、太阳能电池的主要材料是高纯度的二氧化硅 |
若图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池,则下列的说法中正确的是( )


| A、图2电池在放电过程中,正极区的电极反应为:BH4--8e-+8OH-═BO2-+6H2O |
| B、若用稀硫酸浸湿滤纸并用导线将a、b相连,则有电子从b极流出通过导线流向a极 |
| C、若用硫酸钠和紫色石蕊的混合溶液浸湿滤纸并用导线将a、b相连,则可看到铅笔芯C点处浸有紫色石蕊的滤纸变蓝,此处发生电极反应为:O2+2H2O+4e-═4OH- |
| D、若用KI-淀粉溶液浸湿滤纸,同时用导线将a、b分别与A、B电极相连,若看到铅笔芯C点处出现变蓝现象,则b极连接的是燃料电池的A极 |
可逆反应2S02(g)+O2(g)?2S03(g),如果υ(S02)=O.05mol/(L?s),用一定的SO2和O2在容积固定的密闭容器内发生反应,则2s后SO3的浓度为( )
| A、0.001mo1/L |
| B、O.1mol/L |
| C、O.01mol/L |
| D、0.6mol/L |
我们所吃的豆腐,主要成分是( )
| A、葡萄糖 | B、蛋白质 |
| C、脂肪 | D、淀粉 |
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、0.5molO3与11.2LO2所含的分子数一定相等 |
| B、标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA |
| C、常温常压下,92g的NO2含有的原子数为6 NA |
| D、1.00mol/L NaCl中,含有Na+的数约为6.02×1023 |
下列各组气体,不论以何种比例混合,同温、同压时,其密度不等于N2的密度的是( )
| A、O2和H2 |
| B、C2H4和CO |
| C、CH4和C3H6 |
| D、O2和Cl2 |