题目内容
13.下列叙述错误的是( )| A. | 氢氧燃料电池是一种将化学能转化为电能的装置 | |
| B. | 铁船舶的外壳上镶嵌锌块,可避免船体遭受腐蚀 | |
| C. | 钢铁腐蚀时负极的电极反应式:Fe-3e-═Fe+ | |
| D. | 工业上电解饱和食盐水时阴极的电极反应式:2H++2e-═H2↑ |
分析 A.燃料电池能向外提供电能;
B.Zn、Fe形成原电池时,Zn失电子被腐蚀;
C.Fe作负极失电子生成亚铁离子;
D.电解饱和食盐水时阴极上阳离子得电子.
解答 解:A.燃料电池能向外提供电能,能把化学能转化为电能,故A正确;
B.Zn、Fe形成原电池时,Zn失电子被腐蚀,Fe作正极被保护,所以铁船舶的外壳上镶嵌锌块,可避免船体遭受腐蚀,故B正确;
C.钢铁腐蚀时Fe作负极失电子生成亚铁离子,则负极的电极反应式:Fe-2e-═Fe2+,故C错误;
D.工业上电解饱和食盐水时,阴极上氢离子得电子生成氢气,则阴极的电极反应式:2H++2e-═H2↑,故D正确.
故选C.
点评 本题考查了原电池原理和电解池原理的应用,题目难度不大,注意把握电极的判断方法和电极方程式的书写,侧重于考查学生对基础知识的掌握情况.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
4.将500mL pH=5的硫酸铜溶液(足量)用惰性电极电解一段时间,溶液pH变为2,若使溶液的浓度、pH与电解前相同,可采取的方法是( )
| A. | 向溶液中加入0.245g Cu(OH)2 | B. | 向溶液中加入0.31gCuCO3 | ||
| C. | 向溶液中加入0.0025 molH2SO4 | D. | 向溶液中加入0.2gCuO |
1.利用如图所示装置(电极均为惰性电极) 可吸收SO2,并制取硫酸和烧碱溶液,下列说法正确的是( )

| A. | 气体W为氧气 | |
| B. | b极与电源的正极相连 | |
| C. | 离子交换膜c为阳离子交换膜 | |
| D. | a极的电极反应为SO2+2H2O-2e-=SO42-+4H+. |
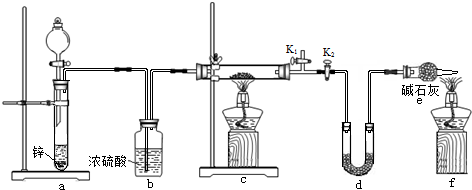
5.下列说法不正确的是( )
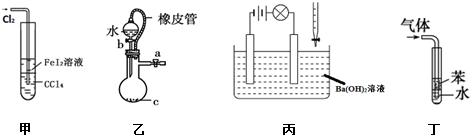

| A. | 甲装置可以用于比较Fe3+、I2、Cl2的氧化性强弱 | |
| B. | 乙装置中打开分液漏斗活塞,水不能顺利流下,说明该装置气密性良好 | |
| C. | 丙装置中若向Ba(OH)2溶液中逐滴加入硫酸溶液直至过量,灯光会由亮变暗至熄灭后又逐渐变亮 | |
| D. | 丁装置不能用于吸收HCl气体及防倒吸 |
2.下列生活小常识或家庭小实验中不涉及化学变化的是( )
| A. | 用食醋去除水垢 | |
| B. | 用竹炭包可清楚衣柜内的异味 | |
| C. | 用铁钉等材料探究铁生锈的条件 | |
| D. | 用柠檬汁涂抹在切开苹果表面可防止苹果变色 |
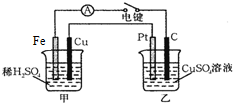 原电池和电解池都能实现能量的置换.回答下列问题:
原电池和电解池都能实现能量的置换.回答下列问题:
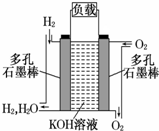 被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效 率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH 溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连 续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效 率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH 溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连 续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题: .
.