题目内容
溴与氯同属“卤族”元素,其单质在性质上具有很大的相似性,但Cl2比Br2的活泼性强,下面是根据氯气的性质,对溴单质性质的预测,其中不正确的是( )
| A、溴单质溶于水得到溴水 |
| B、溴单质与烧碱溶液不反应 |
| C、溴单质与氢气反应的产物为溴化氢,其水溶液具有强酸性 |
| D、溴离子可以用硝酸酸化过的AgNO3溶液来检验 |
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:Cl2比Br2的活泼性强,但二者性质相似,均与水、碱发生氧化还原反应,对应离子均与硝酸银溶液反应生成沉淀,以此来解答.
解答:
解:A.氯气溶于水得到氯水,则溴单质溶于水得到溴水,故A正确;
B.氯气与碱反应,则溴单质与烧碱溶液反应生成NaBr、NaBrO,故B错误;
C.氯气与氢气反应生成HCl,水溶液为强酸溶液,则溴单质与氢气反应的产物为溴化氢,其水溶液具有强酸性,故C正确;
D.氯离子用硝酸酸化过的AgNO3溶液来检验,则溴离子可以用硝酸酸化过的AgNO3溶液来检验,只是沉淀的颜色不同,故D正确;
故选B.
B.氯气与碱反应,则溴单质与烧碱溶液反应生成NaBr、NaBrO,故B错误;
C.氯气与氢气反应生成HCl,水溶液为强酸溶液,则溴单质与氢气反应的产物为溴化氢,其水溶液具有强酸性,故C正确;
D.氯离子用硝酸酸化过的AgNO3溶液来检验,则溴离子可以用硝酸酸化过的AgNO3溶液来检验,只是沉淀的颜色不同,故D正确;
故选B.
点评:本题考查卤素单质的性质,为高频考点,把握性质的相似性为解答的关键,注意把握类推法分析解答,侧重元素化合物知识的考查,题目难度不大.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
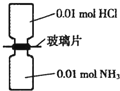 室温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是(设NA表示阿伏加德罗常数的值)( )
室温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是(设NA表示阿伏加德罗常数的值)( )| A、反应前气体的总体积为0.448L |
| B、装置中氢元素的总质量为0.04g |
| C、生成物中含有0.01NA个分子 |
| D、生成物完全溶于水后所得溶液含有0.01 NA个NH4+ |
下列化学用语表述正确的是( )
| A、蔗糖的分子式:C6H12O6 |
B、NH3的电子式: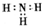 |
C、甲烷的比例模型: |
| D、二氧化碳的结构式:O-C-O |
在18℃时,H2SO3的Kl=1.5×10-2、K2=1.0×10-7,H2S的Kl=9.1×10-8、K2=1.1×10-12,则下列说法中正确的是( )
| A、亚硫酸的酸性弱于氢硫酸 |
| B、亚硫酸溶液的酸性一定强于氢硫酸溶液 |
| C、氢硫酸的酸性弱于亚硫酸 |
| D、多元弱酸的酸性主要由第二步电离决定 |
“纳米材料”是当今材料科学研究的前沿,1纳米(nm)=10-9m,其研究成果广泛应用与催化及军事科学中.“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料.下列分散系中,分散质的微粒直径与“纳米材料”具有相同数量级的是( )
| A、胶体 | B、悬浊液 |
| C、乳浊液 | D、溶液 |
下列反应中属于氧化还原反应的是( )
| A、CO2+2NaOH═Na2CO3+H2O |
| B、CuO+2HCl═CuCl2+H2O |
| C、CaCO3+2HCl═CaCl2+H2O+CO2↑ |
| D、2Na+2H2O═2NaOH+H2↑ |
将表面积和体积均相等的大理石,分别投入过量的甲溶液(0.1mol/L HCl)与乙溶液(0.1mol/L醋酸)中,则( )
| A、初始的速率甲、乙相同,生成二氧化碳的总量甲、乙也相同 |
| B、初始的速率甲大于乙,生成二氧化碳的总量也是甲大于乙 |
| C、初始的速率甲大于乙,生成二氧化碳的总量甲、乙相同 |
| D、反应速率和生成二氧化碳的总量均不相同 |
下列关于阿佛加德罗常数(NA)说法正确的是( )
| A、常温常压下,当活泼金属转移2NA个电子时,可从盐酸中置换产生22.4LH2 |
| B、1mol氯气与足量的氢氧化钠反应,共转移了NA的电子 |
| C、标准状况下,2.24L甲烷和氨气的混合气中所含的电子数为NA |
| D、1mol/L的Na2S溶液中,含有的S2-的数目小于NA |