题目内容
用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 向溶液中加入KSCN溶液,观察无明显现象,继续加入氯水,溶液变红色 | 含有Fe2+溶液 |
| B | 向溶液中加入盐酸,产生使澄清石灰水变浑浊的无色无味气体 | 含有CO32-溶液 |
| C | 通入CO2,溶液变浑浊.再加入品红溶液,红色褪去. | 可能为Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊. | 可能为Ca(OH)2溶液 |
| A、A | B、B | C、C | D、D |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:A.向溶液中加入KSCN溶液,观察无明显现象,说明不含Fe3+,继续加入氯水,溶液变红色,说明生成Fe3+;
B.也可能含有HCO3-;
C.通入CO2,溶液变浑浊.再加入品红溶液,红色褪去,说明生成具有漂白性的物质,且酸性比碳酸弱;
D.通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊,可说明生成Ca(HCO3)2,与NaOH反应生成CaCO3.
B.也可能含有HCO3-;
C.通入CO2,溶液变浑浊.再加入品红溶液,红色褪去,说明生成具有漂白性的物质,且酸性比碳酸弱;
D.通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊,可说明生成Ca(HCO3)2,与NaOH反应生成CaCO3.
解答:
解:A.向溶液中加入KSCN溶液,观察无明显现象,说明不含Fe3+,继续加入氯水,溶液变红色,说明生成Fe3+,可说明原溶液含有Fe2+,故A不选;
B.无色无味气体为二氧化碳,与盐酸反应生成二氧化碳气体,也可能含有HCO3-,故B选;
C.通入CO2,溶液变浑浊.再加入品红溶液,红色褪去,说明生成具有漂白性的物质,且酸性比碳酸弱,可能为Ca(ClO)2溶液,故C不选;
D.通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊,可说明生成Ca(HCO3)2,与NaOH反应生成CaCO3,可能为Ca(OH)2溶液,故D不选.
故选B.
B.无色无味气体为二氧化碳,与盐酸反应生成二氧化碳气体,也可能含有HCO3-,故B选;
C.通入CO2,溶液变浑浊.再加入品红溶液,红色褪去,说明生成具有漂白性的物质,且酸性比碳酸弱,可能为Ca(ClO)2溶液,故C不选;
D.通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊,可说明生成Ca(HCO3)2,与NaOH反应生成CaCO3,可能为Ca(OH)2溶液,故D不选.
故选B.
点评:本题考查物质的检验和鉴别,为高频考点,侧重学生的分析、实验能力的考查,注意把握物质的性质的差异以及实验的严密性和评价,难度不大.

练习册系列答案
相关题目
将一定量的NaHCO3和NH4HCO3的混合物放入坩埚内,用酒精加热到质量不变时,最终称得残留物得质量是原来的一半,则原混合物中NH4HCO3的质量数为 ( )
| A、25% |
| B、20.75% |
| C、17.85% |
| D、26.45% |
工业上由重晶石制取可溶性钡盐,对已经粉碎后的矿石首先进行的处理方法应是( )
| A、水溶法 | B、酸溶法 |
| C、碱溶法 | D、还原法 |
下列除杂质(括号内为杂质)方法合理的是( )
| A、Fe3+(Fe2+),加过量铁粉,过滤 |
| B、Mg2+(Al3+),加过量氨水,过滤 |
| C、CO2(HCl),通过碳酸钠饱和溶液,洗气 |
| D、固体Na2CO3(NaHCO3),加热至恒重 |
有4种碳架如下的烃( )


| A、a和c是同分异构体 |
| B、a和d是同分异构体 |
| C、a和d都能发生加成反应 |
| D、只有b和c能发生加成反应 |

 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: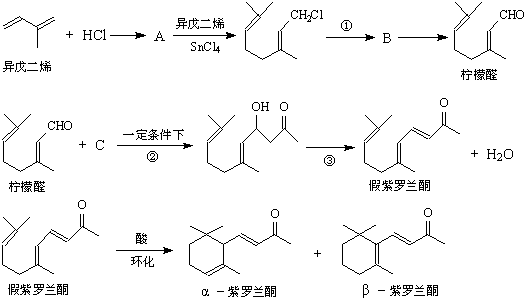
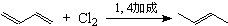
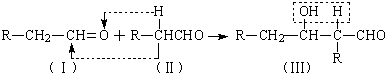
 .
.

