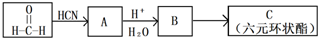
题目内容
水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+).下列对上述过程的描述不合理的是( )
| A、氧原子的杂化类型发生了改变 |
| B、微粒的形状发生了改变 |
| C、微粒的化学性质发生了改变 |
| D、微粒中的键角发生了改变 |
考点:原子轨道杂化方式及杂化类型判断,判断简单分子或离子的构型
专题:化学键与晶体结构
分析:水分子中氧原子的杂化为sp3,H3O+中氧原子的杂化为sp3,水分子为V形结构,H3O+为三角锥形结构,据此分析解答.
解答:
解:A、水中氧的杂化为sp3,H3O+中氧的杂化为sp3,则氧原子的杂化类型没有改变,故A不合理;
B、水分子为V型,H3O+为三角锥型,则微粒的形状发生了改变,故B合理;
C、因结构不同,则性质不同,微粒的化学性质发生了改变,故C合理;
D、水分子为V型,H3O+为三角锥型,微粒中的键角发生了改变,故D合理;
故选A.
B、水分子为V型,H3O+为三角锥型,则微粒的形状发生了改变,故B合理;
C、因结构不同,则性质不同,微粒的化学性质发生了改变,故C合理;
D、水分子为V型,H3O+为三角锥型,微粒中的键角发生了改变,故D合理;
故选A.
点评:本题考查了微粒的结构、性质、原子杂化方式等知识点,根据价层电子对互斥理论确定其原子杂化方式、微粒结构,再结合结构确定性质、键角等知识点,题目难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
粗略测定草木灰中碳酸钾的含量并检验钾元素的存在,图示中涉及的对应操作不规范的是( )
A、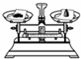 称量 |
B、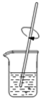 溶解 |
C、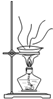 蒸发 |
D、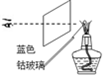 焰色反应 |
Na2S溶液中各种离子的物质的量浓度关系不正确的是( )
| A、c(Na+)>c(S2-)>c(HS-)>c(OH-) |
| B、c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-) |
| C、c(Na+)=2c(HS-)+2c(S2-)+2c(H2S) |
| D、c(OH-)=c(H+)+c(HS-) |
下列关于有机物的说法正确的是( )
| A、聚乙烯可发生加聚反应 |
| B、塑料、橡胶、合成纤维都属于有机高分子化合物 |
| C、淀粉、蛋白质的水解产物互为同分异构体 |
| D、乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
科学家研制出多种新型杀虫剂代替DDT,化合物A是其中一种.下列关于化合物A的说法不正确的是( )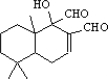

| A、化合物A属于酚类物质 |
| B、能发生取代反应 |
| C、分子中最少有5个碳原子共平面 |
| D、化合物A可以发生加成反应 |

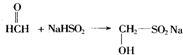 ,回答下列问题:
,回答下列问题: