题目内容
设NA为阿伏伽德罗常数,下列说法正确的是( )
| A、标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA |
| B、7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA |
| C、25℃时,1LpH=13的氢氧化钠溶液中含有NA个氢氧根离子 |
| D、在常压、温室条件下,1mol氦气含有的原子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.注意辛烷的状态;
B.先计算氯气的物质的量,再根据反应式计算转移电子数;
C.根据PH计算氢离子浓度,再根据水的离子积计算氢氧根离子浓度,再由体积计算氢氧根个数;
D.氦气为单原子分子.
B.先计算氯气的物质的量,再根据反应式计算转移电子数;
C.根据PH计算氢离子浓度,再根据水的离子积计算氢氧根离子浓度,再由体积计算氢氧根个数;
D.氦气为单原子分子.
解答:
解:A.在标准状况下,辛烷为液态,不能用22.4L/mol来计算辛烷的物质的量为,故A错误;
B.7.1g氯气的物质的量为0.1mol,氯气和碱反应的方程式为:Cl2+2OH-=Cl-+ClO-+H2O,0.1mol氯气和碱反应转移电子数为0.1NA,故B错误;
C.pH=13的氢氧化钠溶液中,氢离子浓度为10-13mol/L,氢氧根离子浓度为:
=0.1mol/L,1L溶液中含氢氧根离子个数为0.1NA,故C错误;
D.氦气为单原子分子,1mol氦气含有的原子数为NA,正确;
故选D.
B.7.1g氯气的物质的量为0.1mol,氯气和碱反应的方程式为:Cl2+2OH-=Cl-+ClO-+H2O,0.1mol氯气和碱反应转移电子数为0.1NA,故B错误;
C.pH=13的氢氧化钠溶液中,氢离子浓度为10-13mol/L,氢氧根离子浓度为:
| 1×10-14 |
| 10-13 |
D.氦气为单原子分子,1mol氦气含有的原子数为NA,正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等.注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,明确标况下气体摩尔体积的使用条件.

练习册系列答案
相关题目
下列反应的离子方程式正确的是( )
| A、醋酸与锌粒反应:2H++Zn=H2↑+Zn2+ | ||||
| B、用FeCl3溶液腐蚀铜板:Cu+Fe3+=Cu2++Fe2+ | ||||
| C、向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ | ||||
D、用石墨电极电解食盐水:2Cl-+2H2O
|
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同.下列分析正确的是( )
| A、脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B、含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
| C、脱氧过程中铁作原电池负极,电极反应为:Fe-3e-=Fe3+ |
| D、脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e-=4OH- |
根据热化学方程式:S(s)+O2(g)=SO2(g)△H=-297.23kJ/mol,下列说法正确的是( )
| A、1molSO2 (g)的能量总和大于1molS(s)和1mol O2(g)的能量总和 |
| B、1molSO2(g)的能量总和小于1molS(s)和1molO2(g)的能量总和 |
| C、S(g)+O2(g)=SO2(g)△H=-Q kJ/mol; Q的值大于297.23 |
| D、S(g)+O2(g)=SO2(g)△H=-Q kJ/mol; Q的值等于297.23 |
下列说法正确的是( )
| A、淀粉和蛋白质它们水解的最终产物都是葡萄糖 |
| B、为防止轮船的船体在海水中被腐蚀,一般在船身连接锌块 |
| C、万一不慎误服重金属盐,应大量吞服鸡蛋清 |
| D、麦芽糖能水解,且最终水解产物有两种 |
下列有关实验操作正确的是( )
A、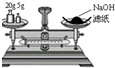 称量氢氧化钠固体 |
B、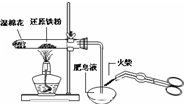 检验铁粉与水蒸气反应产生的氢气 |
C、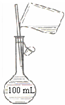 配制150 mL 0.10 mol/L盐酸 |
D、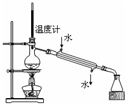 分离两种互溶但沸点相差较大的液体混合物 |
下列有关金属的说法正确的是( )
| A、金属原子的核外电子在金属晶体中都是自由电子 |
| B、镁型和铜型的原子堆积方式空间利用率最高 |
| C、金属原子在化学变化中失去的电子数越多,其还原性越强 |
| D、温度升高,金属的导电性将变强 |
下列物质互为同素异形的是( )
| A、CaCO3和MgCO3 |
| B、CO和CO2 |
| C、C60 和C70 |
| D、1H和2H |
下列说法正确的是( )
| A、放热的反应在常温下一定易进行 |
| B、吸热反应在常温下不能进行 |
| C、有吸热或放热现象的过程中一定发生了化学反应 |
| D、反应是放热还是吸热是由反应物和生成物所具有的能量的相对大小决定的 |