题目内容
如图所示,△H1=-393.5kJ?mol-1△H2=-395.4kJ?mol-1,下列说法或表示式正确的是( )
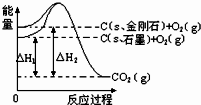
| A.C(s、石墨)=C(s、金刚石)△H=+1.9kJ?mol-1 |
| B.石墨的能量比金刚石高 |
| C.金刚石的稳定性强于石墨 |
| D.金刚石燃烧的热化学方程式为:C(s、金刚石)+O2(g)=CO2(g)△H=395.4kJ?mol-1 |

由图得:①C(S,石墨)+O2(g)=CO2(g)△H=-393.5kJ?mol-1
②C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJ?mol-1,
利用盖斯定律将①-②可得:C(S,石墨)=C(S,金刚石)△H=+1.9kJ?mol-1,则
A、因C(s、石墨)=C(s、金刚石)△H=+1.9kJ?mol-1,故A正确;
B、石墨转化为金刚石吸热,金刚石能量大于石墨的总能量,故B错误;
C、金刚石能量大于石墨的总能量,物质的量能量越大越不稳定,则石墨比金刚石稳定,故C错误;
D、由图可知金刚石燃烧的热化学方程式为:C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJ?mol-1,故D错误;
故选:A.
②C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJ?mol-1,
利用盖斯定律将①-②可得:C(S,石墨)=C(S,金刚石)△H=+1.9kJ?mol-1,则
A、因C(s、石墨)=C(s、金刚石)△H=+1.9kJ?mol-1,故A正确;
B、石墨转化为金刚石吸热,金刚石能量大于石墨的总能量,故B错误;
C、金刚石能量大于石墨的总能量,物质的量能量越大越不稳定,则石墨比金刚石稳定,故C错误;
D、由图可知金刚石燃烧的热化学方程式为:C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJ?mol-1,故D错误;
故选:A.

练习册系列答案
相关题目
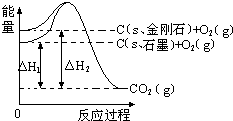 如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示式正确的是( )
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示式正确的是( ) 如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示式正确的是( )
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示式正确的是( )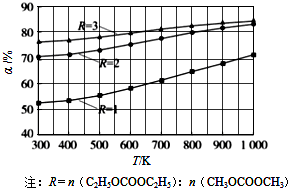 (2012?广州一模)碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液,生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)△H1
(2012?广州一模)碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液,生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)△H1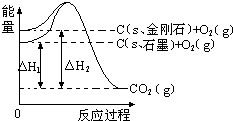 如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示中,正确的是( )
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示中,正确的是( )