题目内容
一种海水电池的反应原理可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,有关该反应的说法正确的是
- A.反应中MnO2是还原剂
- B.Ag的还原性比Na2Mn5O10强
- C.该反应中MnO2具有催化作用
- D.每生成1 mol Na2Mn5O10转移1 mol电子
B
解析:
根据方程式可知,锰的化合价从+4价降低到+3.6价,所以二氧化锰是氧化剂,选项A、C都不正确;在氧化还原反应中还原剂的还原性强于还原产物的,所以选项B正确;每生成1 mol Na2Mn5O10转移2 mol电子,选项D不正确,答案选B。
解析:
根据方程式可知,锰的化合价从+4价降低到+3.6价,所以二氧化锰是氧化剂,选项A、C都不正确;在氧化还原反应中还原剂的还原性强于还原产物的,所以选项B正确;每生成1 mol Na2Mn5O10转移2 mol电子,选项D不正确,答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
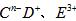 具有相同的电子层结构,E、F的质子数之和是
具有相同的电子层结构,E、F的质子数之和是 电于数的3倍。试回答下列问题:
电于数的3倍。试回答下列问题: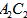 的电子式为_____________________________。
的电子式为_____________________________。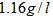 ,已知2克Y完全燃烧可以放出
,已知2克Y完全燃烧可以放出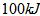 量,写出表示Y燃烧热的热化学方程式:
量,写出表示Y燃烧热的热化学方程式: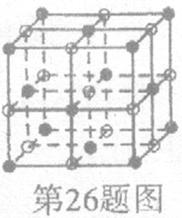
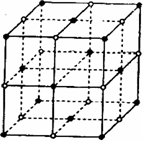
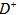 距离最近且相等的
距离最近且相等的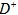 离子个数为_____________。
离子个数为_____________。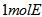 的最高价氧化物的水化物用适量的稀硫酸恰好溶解后,再加人1mol/L的D的最高价氧化物的水化物的水溶液后,生成沉淀39g。则加入1mol/L的D的最高价氧化物的水化物的水溶液的体积可能为____________________________________。
的最高价氧化物的水化物用适量的稀硫酸恰好溶解后,再加人1mol/L的D的最高价氧化物的水化物的水溶液后,生成沉淀39g。则加入1mol/L的D的最高价氧化物的水化物的水溶液的体积可能为____________________________________。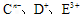 具有相同的电子层结构,E、F的质子数之和是
具有相同的电子层结构,E、F的质子数之和是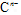 电子数的3倍。试回答下列问题:
电子数的3倍。试回答下列问题: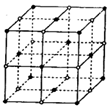
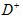 距离最近且相等的
距离最近且相等的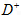 离子个数为_____________。
离子个数为_____________。