题目内容
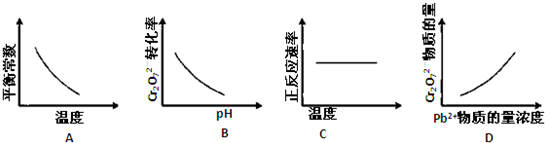
下列反应△H<0的是( )
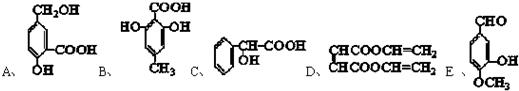
A、、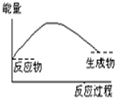 |
B、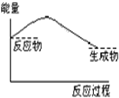 |
C、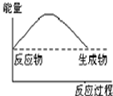 |
D、、 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:△H=生成物的能量和-反应物的能量和,反应物能量高于生成物时反应放热,反之吸热,据此解答.
解答:
△H=生成物的能量和-反应物的能量和,反应物能量高于生成物时反应放热,反之吸热,
A、反应物能量低于生成物,反应吸热,△H>0,故A错误;
B、反应物能量高于生成物,反应放热,△H<0,故B正确;
C、不存在反应物和生成物能量相同的反应,故C错误;
D、反应过程中能量升高,因为,需要拆开反应物的化学键,吸收能量,也就是反应的活化能,不可能降低,故D错误.
故选:B.
A、反应物能量低于生成物,反应吸热,△H>0,故A错误;
B、反应物能量高于生成物,反应放热,△H<0,故B正确;
C、不存在反应物和生成物能量相同的反应,故C错误;
D、反应过程中能量升高,因为,需要拆开反应物的化学键,吸收能量,也就是反应的活化能,不可能降低,故D错误.
故选:B.
点评:本题通过图象考查反应物和生成物能量高低决定反应放热还是吸热,以及活化能的含义.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、固体NaCl不导电,但 NaCl是电解质 |
| B、CO2的水溶液导电,但 CO2不是电解质 |
| C、铜、石墨均导电,但它们均不是电解质 |
| D、稀硫酸能导电,所以稀硫酸是电解质 |
下列轨道表示式能表示磷原子的最低能量状态的是( )
A、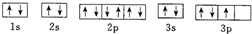 |
B、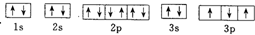 |
C、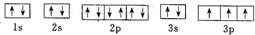 |
D、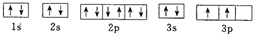 |
下列物质分类正确的是( )
| A、SO2、SiO2、CO2、CO均为酸性氧化物 |
| B、稀豆浆、硅酸、水玻璃、氯化铁溶液均为胶体 |
| C、烧碱、冰醋酸、四氯化碳、NH3均为电解质 |
| D、BaSO4的水溶液不导电,但BaSO4是强电解质 |
 已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.
已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.