题目内容
1.下列说法中错误的是( )| A. | 乙醇分子结构中不存在手性碳 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | SO2、SO3都是极性分子 | |
| D. | 原子晶体中原子以共价键结合,具有键能大、硬度大的特性 |
分析 A、根据有机分子中碳原子连四个不同的原子或原子团判断;
B、NH4+中氮原子提供孤电子对,氢原子提供空轨道,从而形成配位键,[Cu(NH3)4]2+中铜原子提供空轨道,氮原子提供孤电子对,所以形成配位键;
C、对于ABn型共价分子,若中心原子A达到了最高正价,没有孤对电子时,为非极性分子,若中心原子未达到最高正价,有孤对电子对,为极性分子;
D、原子晶体中,组成晶体的微粒是原子,原子间的相互作用是共价键,共价键结合牢固,原子晶体的熔、沸点高,硬度大,不溶于一般的溶剂,多数原子晶体为绝缘体.
解答 解:A、乙醇分子中有一个碳连3个相同的氢,还有一个连2个相同的氢,所以无手性碳,故A正确;
B、NH4+中氮原子提供孤电子对,氢原子提供空轨道,从而形成配位键;[Cu(NH3)4]2+中铜原子提供空轨道,氮原子提供孤电子对,所以形成配位键,故B正确;
C、SO2中心原子S的化合价为+4价,最外层电子未全部参与成键,含有孤对电子对,为极性分子;SO3中心原子S的化合价为+6价,最外层电子全部参与成键,没有孤对电子对,SO3是平面三角形的分子,是非极性分子,故C错误;
D、原子晶体中相邻原子间以共价键结合而形成的空间网状结构的晶体,共价键结合牢固,原子晶体的熔、沸点高,硬度大,故D正确.
故选C.
点评 本题综合性较大,涉及分子极性、配位键、手性碳、晶体结构与性质,难度不大,注意基础知识的掌握.

练习册系列答案
相关题目
12.一定条件下,乙醛可发生分解:CH3CHO(l)→CH4+CO,已知该反应的活化能为190kJ.mol-1,在含有少量I2的溶液中,该反应的机理为:( )
反应Ⅰ:CH3CHO+I2→CH3I2+HI+CO
反应Ⅱ:CH3I+HI→CH4+I2 .
反应Ⅰ:CH3CHO+I2→CH3I2+HI+CO
反应Ⅱ:CH3I+HI→CH4+I2 .
| A. | 反应速率与I2的浓度有关 | |
| B. | HI在反应Ⅰ中是氧化产物 | |
| C. | 反应焓变的绝对值等于190kJ•mol-1 | |
| D. | 乙醛的反应速率主要取决于反应Ⅱ |
6.有①甲烷分子;②氨分子;③白磷分子;④氯仿分子;⑤四氯化碳分子;⑥二氧化碳分子.其中不是四面体构型的是( )
| A. | ①③ | B. | ③⑤ | C. | ①⑤ | D. | ②⑥ |
13.已知有机物A、B之间存在转化关系:A(C6H12O2)+H2O$?_{△}^{稀硫酸}$B+CH3COOH(已配平).则符合条件的B的同分异构体有(不考虑立体异构)( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
10.用下列实验装置进行相应实验,装置正确且能达到实验目的是( )
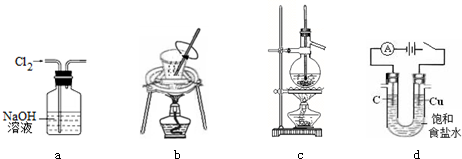

| A. | 用图a所示装置除去Cl2中含有的HCl | |
| B. | 用图b所示装置进行从海带中提取碘实验时灼烧海带 | |
| C. | 用图c所示装置分离沸点相差较大的互溶液体混合物 | |
| D. | 用图d所示装置进行电解法制Cl2、H2 |
11.根据图,下列判断中正确的是( )
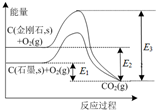

| A. | 石墨与O2生成CO2的反应是吸热反应 | |
| B. | 等量金刚石和石墨完全燃烧,金刚石放出热量更多 | |
| C. | 从能量角度看,金刚石比石墨更稳定 | |
| D. | 金刚石转化为石墨需要吸收的能量为E3-E2 |
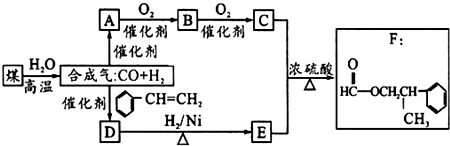
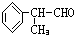
 .
. 、
、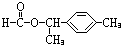 .
.
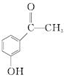 .
.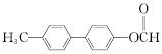 .
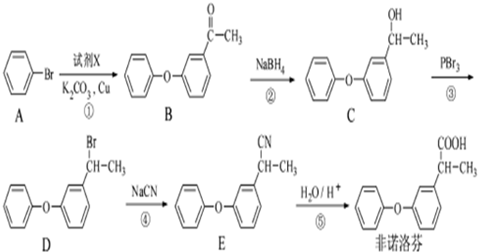
.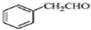 为原料制备
为原料制备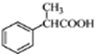 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: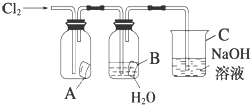 某同学按图进行实验,在A中放的是干燥的红色纸条,B中放的是湿润的红色纸条,C中盛放的是氢氧化钠溶液.请回答下列问题.
某同学按图进行实验,在A中放的是干燥的红色纸条,B中放的是湿润的红色纸条,C中盛放的是氢氧化钠溶液.请回答下列问题.