题目内容
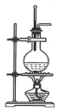
15.某校化学兴趣小组为探究铁与浓硫酸的反应,设计了图1、图2所示装置进行实验.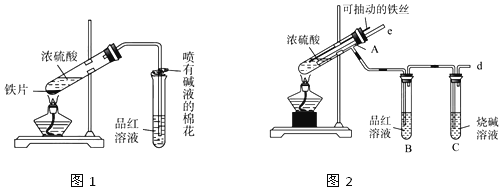
(1)比较两个实验装置,图2装置的优点是:
①能更好的吸收有毒气体SO2防止其污染环境;
②便于控制反应的发生和停止.
(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到”液封”作用阻止SO2气体逸出而防止污染环境;二是停止加热时,防止倒吸或平衡压强. 能说明有SO2气体产生的实验现象是品红溶液褪色.
(3)(反应一段时间后,用滴管吸取A试管中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+.
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
A.稀HCl溶液 B.稀硫酸 C.KSCN溶液 D.酸性KMnO4溶液
E.NaOH溶液 F.淀粉KI溶液 G. H2O2溶液
验证Ⅱ:取试样,先滴加少量的C (填试剂序号,下同),振荡,再滴加少量的G,根据溶液颜色的变化可确定假设Ⅱ是否正确.
验证Ⅲ:步骤1.取试样,滴加少量的C(或F) (填试剂序号),溶液的颜色变红(或蓝) 色,则试样中含有Fe3+发生反应的离子方程式为Fe3++3SCN-═Fe(SCN)3或2I-+2Fe3+=I2+2Fe2+.
步骤2.再取适量的试样滴加少量的D (填试剂序号),溶液颜色的变化为酸性KMnO4溶液的浅红色褪去,则试样中含有Fe2+.
分析 (1)图2装置中Fe丝可以抽动,能控制反应的发生和停止,有尾气处理装置;
(2)导气管e与外界连通能起到平衡压强防止倒吸的作用;根据检验二氧化硫的方法分析;
(3)验证Ⅱ:检验Fe2+,先加KSCN溶液,再加H2O2溶液;
验证Ⅲ:步骤1.检验Fe3+,加KSCN溶液,变红色;或加淀粉KI溶液,变蓝色;
步骤2.既有Fe3+又有Fe2+时,检验Fe2+要加酸性KMnO4溶液.
解答 解:(1)图2装置中Fe丝可以抽动,能控制反应的发生和停止,而且有尾气处理装置,
故答案为:便于控制反应的发生和停止;
(2)导气管e与外界连通能起到平衡压强防止倒吸的作用;二氧化硫具有漂白性,能是品红溶液褪色,
故答案为:停止加热时,能防止倒吸或平衡压强;品红溶液褪色;
(3)验证Ⅱ:检验Fe2+,先加KSCN溶液,再加H2O2溶液;
故答案为:C,G;
验证Ⅲ:步骤1.检验Fe3+,加KSCN溶液,变红色,发生的反应为:Fe3++3SCN-═Fe(SCN)3;或加淀粉KI溶液,变蓝色,其反应为:2I-+2Fe3+=I2+2Fe2+;
故答案为:C(或F);红(或蓝);Fe3++3SCN-═Fe(SCN)3或2I-+2Fe3+=I2+2Fe2+;
步骤2.既有Fe3+又有Fe2+时,检验Fe2+要加酸性KMnO4溶液,高锰酸钾溶液褪色证明有二价铁离子,
故答案为:D;酸性KMnO4溶液的浅红色褪去.
点评 本题考查性质方案的设计,题目难度中等,明确常见元素及其化合物性质为解答关键,注意掌握性质方案设计的原则,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
1.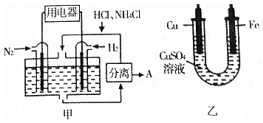 如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.
如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.
下列说法中正确的是( )
 如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.
如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.下列说法中正确的是( )
| A. | 通入H2-极与图乙中的铜电极相连 | |
| B. | 电池工作一段时间后,溶液pH减少1 | |
| C. | 当消耗0.025molN2时,则铁电极增重1.6g | |
| D. | 通入N2-端的电极反应式为:N2+8H++6e-═2NH4+ |
2.下列各组微粒的空间构型相同的是( )
①NH3和H2O
②NH4+和H3O+
③NH3和H3O+
④O3和SO2
⑤CO2和C2H2
⑥SiO44-和ClO4-.
①NH3和H2O
②NH4+和H3O+
③NH3和H3O+
④O3和SO2
⑤CO2和C2H2
⑥SiO44-和ClO4-.
| A. | 全部 | B. | 除①④⑥以外 | C. | ③④⑤⑥ | D. | ②⑤⑥ |
3.当足量的CO通过玻璃管内灼热的某一氧化物后,充分反应,管内物质质量减少了27.5%,则氧化物为( )
| A. | CuO | B. | MnO2 | C. | Fe2O3 | D. | Fe3O4 |
10.(1)在同一个原子中,离核越近、n越小的能层中的电子能量越低.理论研究证明,多电子原子中,同一能层的电子,能量也可能不同,还可以把它们分成能级,第三能层有3个能级,分别为3s、3p和3d.现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,处于最低能量的原子叫做基态原子.
(2)写出下列基态原子的简化电子排布式:
①14Si1s22s22p63s23p2 或[Ne]3s23p2;②26Fe1s22s22p63s23p63d64s2或[Ar]3d64s2 .
(3)按所示格式填写表中的空格:
(4)N≡N的键能为942kJ•mol-1,N-N单键的键能为247kJ•mol-1,计算说明N2中的π键更稳定(填“σ”或“π”).
(5)在配离子[Fe(SCN)]2+中,提供空轨道接受孤电子对的微粒是Fe3+,配离子[Cu(NH3)4]2+的配体是NH3.
(6)根据价层电子对互斥理论判断:
①NH3分子中,中心原子上的σ键电子对数为3,孤电子对数为1,价层电子对数为4,中心原子的杂化方式为sp3杂化,VSEPR构型为四面体形,分子的立体构型为三角锥形.
②BF3分子中,中心原子的杂化方式为sp2杂化,分子的立体构型为平面(正)三角形.
(2)写出下列基态原子的简化电子排布式:
①14Si1s22s22p63s23p2 或[Ne]3s23p2;②26Fe1s22s22p63s23p63d64s2或[Ar]3d64s2 .
(3)按所示格式填写表中的空格:
| 原子序数 | 原子的价电子排布式 | 周期 | 族 |
| 17 | 第三 | ||
| 3d54s1 | ⅥB |
(5)在配离子[Fe(SCN)]2+中,提供空轨道接受孤电子对的微粒是Fe3+,配离子[Cu(NH3)4]2+的配体是NH3.
(6)根据价层电子对互斥理论判断:
①NH3分子中,中心原子上的σ键电子对数为3,孤电子对数为1,价层电子对数为4,中心原子的杂化方式为sp3杂化,VSEPR构型为四面体形,分子的立体构型为三角锥形.
②BF3分子中,中心原子的杂化方式为sp2杂化,分子的立体构型为平面(正)三角形.
7.下列有关说法正确的是( )
| A. | 明矾既可用作净水剂,也可用作消毒剂 | |
| B. | 小苏打、氢氧化铝都可用于治疗胃酸过多 | |
| C. | 煤的干馏、石油的分馏都属于化学变化 | |
| D. | 已知PM2.5是指大气中直径小于或等于2.5微米(1微米=1000纳米)的颗粒物,则PM2.5在空气中能形成胶体 |