题目内容
下列有关说法正确的是( )
| A、将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
| B、室温下,饱和氯水中能大量存在C1-、Fe3+、NO3-、Na+、SO32- |
| C、浓度和体积相同的NaOH和CH3COOH相混合,溶液中c(Na+)>c(CH3COO-) |
| D、放电反应为H2+2NiO(OH)=2Ni(OH)2的电池,充电时,阴极上NiO(OH)被还原 |
考点:原电池和电解池的工作原理,离子浓度大小的比较,离子共存问题
专题:
分析:A.在溶液中NH3与Cu2+不发生氧化还原反应;
B.氯水具有强氧化性能氧化SO32-;
C.CH3COO-在溶液中水解,CH3COO-的浓度减小;
D.根据电极反应物判断.
B.氯水具有强氧化性能氧化SO32-;
C.CH3COO-在溶液中水解,CH3COO-的浓度减小;
D.根据电极反应物判断.
解答:
解:A.在溶液中NH3与Cu2+不发生氧化还原反应,将NH3通入热的CuSO4溶液中会生成氢氧化铜沉淀,故A错误;
B.饱和氯水中含有氯气和次氯酸,二者都具有强氧化性能氧化SO32-,所以不能存在SO32-,故B错误;
C.浓度和体积相同的NaOH和CH3COOH相混合,恰好生成CH3CONa,CH3COO-在溶液中水解,CH3COO-的浓度减小,所以溶液中c(Na+)>c(CH3COO-),故C正确;
D.放电反应为H2+2NiO(OH)=2Ni(OH)2的电池,充电时,要生成H2,则H元素得电子生成H2,故D错误.
故想C.
B.饱和氯水中含有氯气和次氯酸,二者都具有强氧化性能氧化SO32-,所以不能存在SO32-,故B错误;
C.浓度和体积相同的NaOH和CH3COOH相混合,恰好生成CH3CONa,CH3COO-在溶液中水解,CH3COO-的浓度减小,所以溶液中c(Na+)>c(CH3COO-),故C正确;
D.放电反应为H2+2NiO(OH)=2Ni(OH)2的电池,充电时,要生成H2,则H元素得电子生成H2,故D错误.
故想C.
点评:本题考查了常见元素化合物物质的性质、盐的水解、电化学知识,题目涉及的知识点较多,题目难度不大,注意对基础知识的积累.

练习册系列答案
相关题目
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:则25℃时,反应X+3Y?2Z的平衡常数为( )
| 物质 | X | Y | Z |
| 初始浓度/mol?L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol?L-1 | 0.05 | 0.05 | 0.1 |
| A、500 |
| B、600 |
| C、1 200 |
| D、1 600 |
某混合溶液中可能含有下列离子中的若干种:K+、Na+、Fe2+、Fe3+、SO42-、NO2-、CO32- 现取三份20mL该溶液进行如下实验.根据上述实验,以下说法正确的是( )
①第一份加入足量稀盐酸,无任何气体产生;
②第二份加入足量NaOH,经搅拌,过滤,洗涤,灼烧,最后得到x g固体;
③第三份滴加0.1mol.L-1酸性KMnO4溶液,反应至终点,共消耗其体积为VmL;
④另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色.
①第一份加入足量稀盐酸,无任何气体产生;
②第二份加入足量NaOH,经搅拌,过滤,洗涤,灼烧,最后得到x g固体;
③第三份滴加0.1mol.L-1酸性KMnO4溶液,反应至终点,共消耗其体积为VmL;
④另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色.
| A、原混合溶液中只存在Na+、Fe3+、SO42-,不可能存在K+、CO32- |
| B、由实验①无法推断原混合溶液中是否含有SO42- |
| C、由实验①、②可判断原混合溶液中是否含有Fe3+ |
| D、由实验③可判断原混合溶液中存在Fe2+ |
化学反应N2+3H2→2NH3的能量变化如图所示,该反应的热化学方程式是( )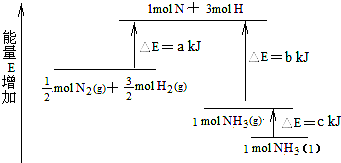
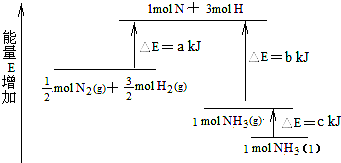
A、
| ||||
B、
| ||||
| C、N2(g)+3 H2(g)→2 NH3(g);△H=2(b-a)kJ/mol | ||||
| D、N2(g)+3 H2(g)→2 NH3(1);)△H=2(a-b-c)kJ/mol |
下列有关说法正确的是 ( )
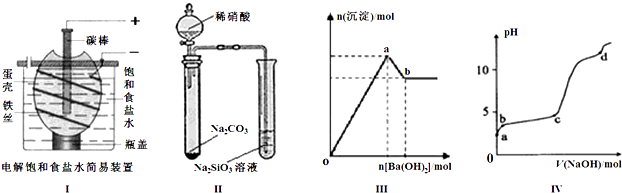

| A、按图Ⅰ装置电解一段时间后,往蛋壳外溶液中滴加几滴酚酞,溶液呈红色 |
| B、按图Ⅱ装置实验,可以证明酸性强弱关系为:硝酸>碳酸>硅酸 |
| C、图Ⅲ表示:向明矾溶液中逐滴加入Ba(OH)2溶液,生成沉淀的物质的量随Ba(OH)2加入量的变化曲线,则oa段发生的离子反应为: 2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| D、图Ⅳ表示:室温时,将1mol?L-1 NaOH溶液逐滴滴入0.2mol?L-1 Al2(SO4)3溶液中,实验测得溶液pH随NaOH溶液体积变化曲线,则d点时Al(OH)3沉淀开始溶解 |
化合物A的分子式为C4H9NO2,A的同分异构体中属于氨基酸的有( )
| A、5种 | B、4种 | C、3种 | D、6种 |
下列说法中,正确的是( )
| A、从碘水中提取碘单质,可选用酒精作有机萃取剂 |
| B、蒸馏操作时,应使温度计的水银球深入液体中 |
| C、与盐酸反应生成CO2,碳酸钠比碳酸氢钠快 |
| D、向Na2CO3和NaHCO3溶液中分别滴加酚酞试液,两者都显红色 |