题目内容
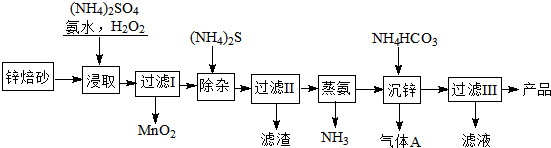
11.锂离子电池的广泛应用使得锂电池的回收利用一直是科学家关注的焦点.磷酸铁锂则是锂电池中最有前景的正极材料,磷酸铁是其前驱体,充放电时可以实现相互转化.某研究性小组对废旧锂离子电池正极材料(图中简称废料,成份为LiFePO4、碳粉和铝箔)进行金属资源回收研究,设计实验流程如图1:已知:①FePO4可溶于稀H2SO4,不溶于水和其他的酸.
②Li2SO4、LiOH和Li2CO3在273K下的溶解度分别为34.2g、22.7g和1.54g373K下,Li2CO3的溶解度为
0.72g
③Ksp[Al(OH)3]=10-32Ksp[Fe(OH)3]=4×10-38
(1)可以提高操作1浸出率的方法有(写出3种)升温,搅拌,增大浓度,增加时间等
(2)完成操作3中的离子方程式:2LiFePO4+H2O2+2H+=2Fe3++2Li++2PO43-+2H2O
(3)该锂电池充电时的正极反应式:LiFePO4 -e-=FePO4+Li+
(4)操作4中应选择试剂NaOH将溶液调节pH值至大于3.2.
(5)沉淀C的成分Li2CO3
(6)磷酸铁也可以通过电解法制备,如右图2,请完成制备过程的总反应离子方程式:Fe2++H2O2+2PO43-=2FePO4+H2O
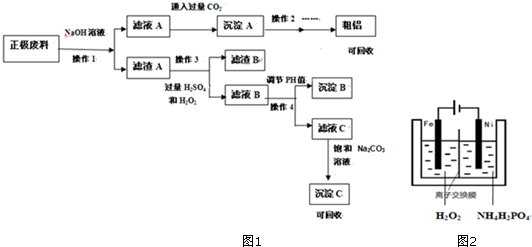
分析 锂离子电池正极材料(成份为LiFePO4、碳粉和铝箔)氢氧化钠溶液溶解,过滤得滤渣A中含有LiFePO4、碳粉,滤液A中含有四羟基合铝酸钠,滤液A中通入二氧化碳得沉淀A为氢氧化铝,氢氧化铝经过灼烧分解、电解可得铝,滤渣A中加入双氧水、硫酸,过滤得滤渣B为碳粉,滤液B的主要成分为Fe3+、Li+、PO43-,调节滤液B的PH值,过滤,可得沉淀B为氢氧化铁,滤液C中含有Li+、PO43-,滤液C中加入碳酸钠可得沉淀C为Li2CO3,据此答题.
解答 解:锂离子电池正极材料(成份为LiFePO4、碳粉和铝箔)氢氧化钠溶液溶解,过滤得滤渣A中含有LiFePO4、碳粉,滤液A中含有四羟基合铝酸钠,滤液A中通入二氧化碳得沉淀A为氢氧化铝,氢氧化铝经过灼烧分解、电解可得铝,滤渣A中加入双氧水、硫酸,过滤得滤渣B为碳粉,滤液B的主要成分为Fe3+、Li+、PO43-,调节滤液B的PH值,过滤,可得沉淀B为氢氧化铁,滤液C中含有Li+、PO43-,滤液C中加入碳酸钠可得沉淀C为Li2CO3,
(1)根据影响反应速率的因素可知,提高操作1浸出率的方法有升温,搅拌,增大浓度,增加时间等,
故答案为:升温,搅拌,增大浓度,增加时间等;
(2)操作3中加入双氧水,将亚铁离子氧化成铁离子,反应的离子方程式为:2LiFePO4+H2O2+2H+=2Fe3++2Li++2PO43-+2H2O,
故答案为:2LiFePO4+H2O2+2H+=2Fe3++2Li++2PO43-+2H2O;
(3)锂电池充电时的正极即为阳极,发生氧化反应,反应式为LiFePO4 -e-=FePO4+Li+,
故答案为:LiFePO4 -e-=FePO4+Li+;
(4)操作4中是调节PH值,使得铁离子沉淀完全,应选择试剂为NaOH,由于Ksp[Fe(OH)3]=4×10-38
,要使铁离子沉淀完全,即c(Fe 3+ )<10-5mol/L,所以此时c(OH- )>$\root{3}{\frac{4×10{\;}^{-38}}{10{\;}^{-5}}}$=$\root{3}{4}$×10-11mol/L,即pH=3.2,所以要将溶液调节pH值至PH>3.2,
故答案为:NaOH;大于3.2;
(5)根据上面的分析可知,沉淀C的成分为Li2CO3,
故答案为:Li2CO3;
(6)磷酸铁也可以通过电解法制备,如右图2,铁作阳极生成亚铁离子,亚铁离子被双氧水氧化成铁离子,再结合磷酸根离子生成磷酸铁,所以制备过程的总反应离子方程式为:Fe2++H2O2+2PO43-=2FePO4+H2O,
故答案为:Fe2++H2O2+2PO43-=2FePO4+H2O.
点评 本题为生产流程题,涉及金属的回收、氧化还原反应、物质的分离、金属的冶炼,有关方程式的计算等问题,题目较为综合,做题时注意仔细审题,从题目中获取关键信息,难度中等.

| A. | 3 mol | B. | $\frac{3}{2}$mol | C. | $\frac{3}{8}$mol | D. | $\frac{8}{3}$mol |
| A. | 用蒸馏水湿润的试纸测某溶液的pH,一定会使结果偏低 | |
| B. | 可用酸式滴定管准确量取10.00mLKMnO4溶液 | |
| C. | 在中和热测定实验中,不能用温度计来搅拌溶液 | |
| D. | 将乙烯通入酸性高锰酸钾溶液,可检验乙烯的还原性 |
下列有关说法正确的是( )
| A. | C2H5OH是氧化剂 | B. | C2H5OH发生氧化反应 | ||
| C. | CrO3是还原剂 | D. | H2SO4是氧化剂 |
| A. | 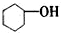 属于醇类 属于醇类 | B. |  属于羧酸 属于羧酸 | C. | 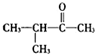 属于酮类 属于酮类 | D. |  属于酚类 属于酚类 |
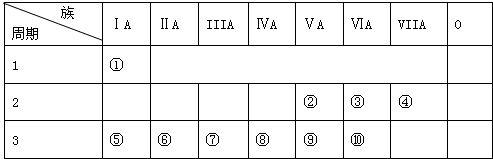
 .
. ,该氢化物的水溶液显碱性(填“酸性”、“碱性”或“中性”),该溶液与少量AlCl3溶液反应的离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
,该氢化物的水溶液显碱性(填“酸性”、“碱性”或“中性”),该溶液与少量AlCl3溶液反应的离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.