题目内容
14.根据下列有关图象,说法正确的是( )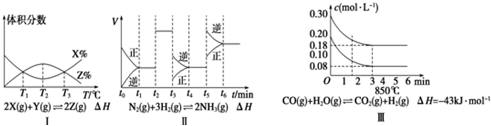
| A. | 由图I知,反应在T1、T3处达到平衡,且该反应的△H<0 | |
| B. | 由图II知,反应在t1时,NH3体积分数最大 | |
| C. | 由图II知,t3时采取的措施是降低反应体系温度 | |
| D. | III在10 L容器、850℃时反应,由图知,到4 min时,反应放出5.16 kJ的热量 |
分析 A、反应物和生成物的体积分数相同时,反应不一定达到平衡状态,升高温度平衡向吸热反应方向移动;
B、t1时刻正逆反应速率相等,反应达到平衡状态;t2时刻正逆反应速率都增大且相等,改变的条件是加入催化剂;t3时刻正逆反应速率都减小,且逆反应速率大于正反应速率,改变的条件是减小压强;t5时刻正逆反应速率都增大,且逆反应速率大于正反应速率,改变的条件是升高温度;
C、降低温度平衡向吸热反应方向移动;
D、根据反应热与反应物物质的量之间的关系式计算.
解答 解:A、由图Ⅰ知,反应在T1、T3处反应物和生成物的体积分数相对但反应不一定达到平衡,T2-T3升高温度,反应物体积分数增大,生成物体积分数减小,平衡向逆反应方向移动,所以正反应是放热反应,△H<0,故A错误;
B、由图Ⅱ知,t2时刻正逆反应速率都增大且相等,改变的条件是加入催化剂,平衡不移动;t3时刻正逆反应速率都减小,且逆反应速率大于正反应速率,改变的条件是减小压强,平衡向逆反应方向移动;t5时刻正逆反应速率都增大,且逆反应速率大于正反应速率,改变的条件是升高温度,平衡向逆反应方向移动,所以反应在t1时,NH3体积分数最大,故B正确;
C、由图Ⅱ知,t3时刻正逆反应速率都减小,且逆反应速率大于正反应速率,改变的条件是减小压强,故C错误;
D、该反应是一个放热反应,1molCO完全转化时放出43KJ能量,当转化(0.30-0.18)mol/L×10L=1.2molCO时放出51.6kJ的热量,故D错误;
故选B.
点评 本题考查了图象分析题,难度较大,分析时注意起点、拐点、转折点等特殊点,然后联系教材中的理论知识,方可做出正确判断.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
2.配制一定物质的量浓度的溶液时,由于操作不慎,使得液面略超过容量瓶的刻度(标线),这时应采取的措施是( )
| A. | 再加点溶质到容量瓶中去 | B. | 影响不大,不再处理 | ||
| C. | 用胶头滴管准确吸出标线上的溶液 | D. | 重新配制 |
9.分子式为C8H8O2并能与饱和NaHCO3溶液反应放出气体的芳香族化合物有(不考虑立体异构)( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
19.下列有关说法或表示正确的是( )
| A. | 淀粉和纤维素都可用(C6H10O5)n表示,二者互为同分异构体 | |
| B. | Mg5(Si4O10)2(OH)2•4H2O的氧化物形式:5MgO•8SiO2•5H2O | |
| C. | Fe-2e-=Fe2+可表示钢铁析氢腐蚀和吸氧腐蚀的正极反应 | |
| D. | 乙醇分子的比例模型: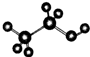 |
6.下列关于阿伏加德罗常数NA的说法正确的是( )
| A. | 8g CH4所含共价键数目为2NA | |
| B. | 0.5NA 个氯气分子与水反应转移电子数为0.5NA | |
| C. | 50mL12mol/L盐酸与足量的MnO2共热,转移的电子数为0.3NA | |
| D. | 1 L0.2mol/L的Na2S溶液中离子数为0.6NA |
3.瓦斯中CH4与O2的质量比为1:4时极易爆炸,此时它们的体积比为( )
| A. | 1:4 | B. | 1:3 | C. | 1:2 | D. | 1:1 |
4.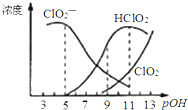 亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析错误的是( )
亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析错误的是( )
 亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析错误的是( )
亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析错误的是( )| A. | HClO2的电离平衡常数的数值Ka=10-6 | |
| B. | 亚氯酸钠在碱性条件下较稳定 | |
| C. | pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c( ClO2)>c( Cl-) | |
| D. | 同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-) |
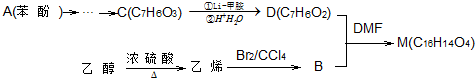
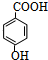

 .
.