题目内容
A、B、C、D四种短周期元素,原子序数依次增大,A、C同主族,C、D同周期,B原子最外层电子数是最内层电子数的3倍.A、B可形成A2B和A2B2两种液态化合物,B、C也可形成C2B和C2B2两种固态化合物.C+具有与氖原子相同核外电子排布.D原子最外层电子数比B原子最外层电子数多一个电子,根据以上条件,判断:
(1)四种元素分别是(写元素符号) A B C D
(2)用电子式写出A2B化合物的形成过程 .
(1)四种元素分别是(写元素符号) A
(2)用电子式写出A2B化合物的形成过程
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:短周期元素,原子序数依次增大,B原子最外层电子数是最内层电子数的3倍,则B为O元素;A、B可形成A2B和A2B2两种液态化合物,则A为H元素;B、C也可形成C2B和C2B2两种固态化合物.C+具有与氖原子相同核外电子排布,则C为Na元素;A、C同主族,C、D同周期,D原子最外层电子数比B原子最外层电子数多一个电子,则D为Cl元素,以此来解答该题.
解答:
解:(1)由短周期元素,原子序数依次增大,B原子最外层电子数是最内层电子数的3倍,则B为2个电子层,质子数为8符合题意,即B为O元素;A、B可形成A2B和A2B2两种液态化合物,化合物为水和过氧化氢,则A为H元素;B、C也可形成C2B和C2B2两种固态化合物,化合物为氧化钠、过氧化钠,C+具有与氖原子相同核外电子排布,则C为Na元素;A、C同主族,C、D同周期,D原子最外层电子数比B原子最外层电子数多一个电子,则D有三个电子层,最外层电子数为7,即D为Cl元素,
故答案为:H;O;Na;Cl;
(2)A2B为水,用电子式表示A2B化合物的形成过程为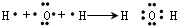 ,
,
故答案为: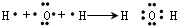 .
.
故答案为:H;O;Na;Cl;
(2)A2B为水,用电子式表示A2B化合物的形成过程为
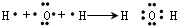 ,
,故答案为:
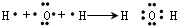 .
.
点评:本题考查位置、结构、性质的关系,明确元素的推断是解答本题的关键,并熟悉物质的性质来解答即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法不正确的是( )
| A、有色玻璃就是由某些胶态金属氧化物分散于玻璃中制成的 |
| B、放射性同位素可用于医疗用品消毒、药物作用机理研究和生物医学研究 |
| C、二氧化氯可用于环保、灭藻、漂白、保鲜、除臭等 |
| D、人体中极少量的NO会促进血管收缩,防止血管扩张 |
在相同条件下,下列气态氢化物的稳定性排列顺序正确的是( )
| A、HF>HCl>HBr>HI |
| B、HCl>HBr>HI>HF |
| C、HBr>HI>HF>HCl |
| D、HI>HBr>HCl>HF |
今有下列三个氧化还原反应:
①2FeCl3+2KI═2FeCl2+2KCl+I2
②2FeCl2+Cl2═2FeCl3
③2KMnO4+16HCl═2KCl+2MnCl2+8H2O+5Cl2↑
若某溶液中有Fe2+和I-共存,要氧化除去I-而又不影响Fe2+和Cl-,可加入的试剂是( )
①2FeCl3+2KI═2FeCl2+2KCl+I2
②2FeCl2+Cl2═2FeCl3
③2KMnO4+16HCl═2KCl+2MnCl2+8H2O+5Cl2↑
若某溶液中有Fe2+和I-共存,要氧化除去I-而又不影响Fe2+和Cl-,可加入的试剂是( )
| A、Cl2 |
| B、KMnO4 |
| C、FeCl3 |
| D、HCl |
下列物质互为同分异构体的一组是( )
| A、CH3OCH3和 CH3CH2OH |
| B、甲烷和乙烷 |
| C、35Cl与37Cl |
| D、白磷和红磷 |

