题目内容
比较下列各组微粒半径,正确的是( )
①Cl<Cl-<Br-②F-<Mg2+<Al3+③Na+<Na<K ④S2-<Cl-<Br-.
①Cl<Cl-<Br-②F-<Mg2+<Al3+③Na+<Na<K ④S2-<Cl-<Br-.
| A、①和③ | B、只有② |
| C、只有③ | D、①和④ |
考点:氧化性、还原性强弱的比较,微粒半径大小的比较
专题:氧化还原反应专题,元素周期律与元素周期表专题
分析:核外电子排布相同,核电荷数越大半径越小;最外层电子数相同,电子层越多半径越大;电子层数相同,核电荷数越大半径越小.据此判断.
解答:
解:①Cl-、Br-最外层电子数相同,Cl-、Br-电子层依次增多,所以离子半径Cl-<Br-,Cl、Cl-电子层数相同,核电荷数相等,核外电子数越多,半径越大,所以Cl<Cl-,故正确;
②Al3+、Mg2+、F-核外电子排布相同,Al3+、Mg2+、F-核电荷数依次减小,所以离子半径Al3+<Mg2+<F-,故错误;
③K电子层最多,所以半径最大,Na、Na+电子层数不相同,Na电子层多,所以,Na>Na+,故正确;
④Br-电子层最多,半径最大,S2-、Cl-的电子层一样,硫离子核电荷数小,所以半径大,即Cl-<S2-<Br-,故错误.
故选:A.
②Al3+、Mg2+、F-核外电子排布相同,Al3+、Mg2+、F-核电荷数依次减小,所以离子半径Al3+<Mg2+<F-,故错误;
③K电子层最多,所以半径最大,Na、Na+电子层数不相同,Na电子层多,所以,Na>Na+,故正确;
④Br-电子层最多,半径最大,S2-、Cl-的电子层一样,硫离子核电荷数小,所以半径大,即Cl-<S2-<Br-,故错误.
故选:A.
点评:考查微粒半径大小比较,难度中等,关键清楚微粒半径大小比较的规律.

练习册系列答案
相关题目
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、常温常压下,18g H2O含有2NA个O-H键 |
| B、1L 1mol/L Na2CO3溶液中含有NA个CO32- |
| C、1mol Al被完全氧化生成Al2O3,转移6NA个电子 |
| D、常温下,22.4L的N2和O2混合气体,含有2NA个原子 |
下列说法中不正确的是( )
| A、乙烯与苯都能使溴水褪色,但褪色原理不同 |
| B、1 mol乙烯与Cl2完全加成,然后与Cl2发生取代反应,共消耗氯气5mol |
| C、溴水遇到乙醛溶液出现褪色现象,是因为它们发生了氧化反应 |
D、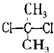 与 与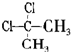 互为同分异构体 互为同分异构体 |
下列叙述中,不正确的是( )
| A、pH=2与pH=1的CH3COOH溶液中,c(H+)之比为1:10 |
| B、1.0mol/L的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| C、仅含Na+、H+、OH-、CH3COO-离子的某溶液中可能存在:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、0.1mol/L的CH3COOH溶液中,由水电离出的c(H+)为1×10-13mol/L |
下列化工生产过程中发生的反应,不属于氧化还原反应的是( )
| A、用氨气制硝酸 |
| B、用石灰石制生石灰 |
| C、用氯气制漂白粉 |
| D、从卤水中提取溴单质 |
 而不是
而不是 ,即假定苯仍具有普通烯烃的性质,则一分子该“环己三烯”在催化剂作用下与一分子H2发生加成反应后产物分子的结构简式是
,即假定苯仍具有普通烯烃的性质,则一分子该“环己三烯”在催化剂作用下与一分子H2发生加成反应后产物分子的结构简式是 某化学实验室需要0.2mol/L NaOH溶液500mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:
某化学实验室需要0.2mol/L NaOH溶液500mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题: