题目内容
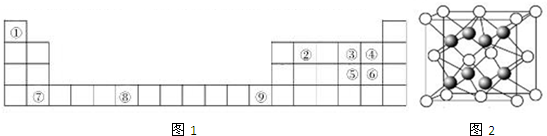
如表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用相应化学用语回答下

列问题:
(l)画出表中形成化合物种类最多元素的原子结构示意图 ;写出它与原予半径最小的原子形成10电子且为正四面体结构的化合物的电子式 ,用电子式表示⑤和⑧形成化合物的过程 .
(2)④⑤⑧形成的简单离子半径由大到小的顺序为 (填离子符号);③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为 (填化学式).
(3)⑤和⑨形成化合物的化学键为 .
(4)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是 (填化学式),写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式 .

列问题:
(l)画出表中形成化合物种类最多元素的原子结构示意图
(2)④⑤⑧形成的简单离子半径由大到小的顺序为
(3)⑤和⑨形成化合物的化学键为
(4)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表位置,可知①为H、②为C、③为N、④为O、⑤为Na、⑥为Al、⑦为Si、⑧为S、⑨为Cl.
(1)形成化合物种类最多元素为碳元素,碳原子核外有2个电子层,各层电子数为2、4;碳元素与原予半径最小的原子形成10电子且为正四面体结构的化合物为CH4,分子中C原子与H原子之间形成1对共用电子对;⑤和⑧形成化合物为Na2S,由钠离子与硫离子构成,用Na原子、S原子电子式表示其形成过程;
(2)电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;非金属性越强最高价含氧酸的酸性越强;
(3)⑤和⑨形成化合物NaCl,由活泼金属与活泼非金属性组成,属于离子化合物;
(4)上述元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是氧化铝;氧化铝与氢氧化钠反应生成偏铝酸钠与水.
(1)形成化合物种类最多元素为碳元素,碳原子核外有2个电子层,各层电子数为2、4;碳元素与原予半径最小的原子形成10电子且为正四面体结构的化合物为CH4,分子中C原子与H原子之间形成1对共用电子对;⑤和⑧形成化合物为Na2S,由钠离子与硫离子构成,用Na原子、S原子电子式表示其形成过程;
(2)电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;非金属性越强最高价含氧酸的酸性越强;
(3)⑤和⑨形成化合物NaCl,由活泼金属与活泼非金属性组成,属于离子化合物;
(4)上述元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是氧化铝;氧化铝与氢氧化钠反应生成偏铝酸钠与水.
解答:
解:由元素在周期表位置,可知①为H、②为C、③为N、④为O、⑤为Na、⑥为Al、⑦为Si、⑧为S、⑨为Cl.
(1)形成化合物种类最多元素为碳元素,碳原子核外有2个电子层,各层电子数为2、4,原子结构示意图为: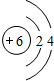 ;碳元素与原予半径最小的原子形成10电子且为正四面体结构的化合物为CH4,分子中C原子与H原子之间形成1对共用电子对,其电子式为:
;碳元素与原予半径最小的原子形成10电子且为正四面体结构的化合物为CH4,分子中C原子与H原子之间形成1对共用电子对,其电子式为: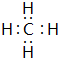 ;⑤和⑧形成化合物为Na2S,由钠离子与硫离子构成,用Na原子、S原子电子式表示其形成过程为:
;⑤和⑧形成化合物为Na2S,由钠离子与硫离子构成,用Na原子、S原子电子式表示其形成过程为: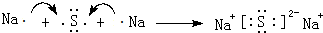 ,
,
故答案为: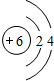 ;
;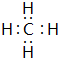 ;
;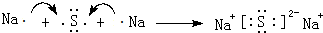 ;
;
(2)电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:S2->O2->Na+;非金属性Cl>N>Si,非金属性越强最高价含氧酸的酸性越强,故酸性:HClO4>HNO3>H2SiO3,故答案为:S2->O2->Na+;HClO4>HNO3>H2SiO3;
(3)⑤和⑨形成化合物NaCl,由活泼金属与活泼非金属性组成,属于离子化合物,含有化学键为离子键,故答案为:离子键;
(4)上述元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是氧化铝,化学式为Al2O3;氧化铝与氢氧化钠反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-=2AlO2-+H2O,
故答案为:Al2O3;Al2O3+2OH-=2AlO2-+H2O.
(1)形成化合物种类最多元素为碳元素,碳原子核外有2个电子层,各层电子数为2、4,原子结构示意图为:
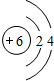 ;碳元素与原予半径最小的原子形成10电子且为正四面体结构的化合物为CH4,分子中C原子与H原子之间形成1对共用电子对,其电子式为:
;碳元素与原予半径最小的原子形成10电子且为正四面体结构的化合物为CH4,分子中C原子与H原子之间形成1对共用电子对,其电子式为: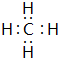 ;⑤和⑧形成化合物为Na2S,由钠离子与硫离子构成,用Na原子、S原子电子式表示其形成过程为:
;⑤和⑧形成化合物为Na2S,由钠离子与硫离子构成,用Na原子、S原子电子式表示其形成过程为: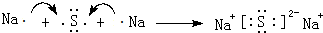 ,
,故答案为:
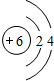 ;
;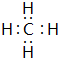 ;
;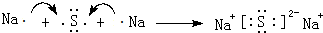 ;
;(2)电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:S2->O2->Na+;非金属性Cl>N>Si,非金属性越强最高价含氧酸的酸性越强,故酸性:HClO4>HNO3>H2SiO3,故答案为:S2->O2->Na+;HClO4>HNO3>H2SiO3;
(3)⑤和⑨形成化合物NaCl,由活泼金属与活泼非金属性组成,属于离子化合物,含有化学键为离子键,故答案为:离子键;
(4)上述元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是氧化铝,化学式为Al2O3;氧化铝与氢氧化钠反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-=2AlO2-+H2O,
故答案为:Al2O3;Al2O3+2OH-=2AlO2-+H2O.
点评:本题考查元素周期表与元素周期律,难度不大,侧重对元素周期律与化学用语考查,注意掌握用电子式表示物质或化学键形成.

练习册系列答案
相关题目
相同温度、相同浓度的溶液,pH值最小的是( )
| A、NH4Cl |
| B、NH4HCO3 |
| C、NH4HSO4 |
| D、(NH4)2 SO4 |
下列说法中正确的是( )
| A、工业上通过设法除去乙醇和氢氧化钠的作用生成的水来制取乙醇钠 |
| B、只使用试管和胶头滴管即可鉴别NaNO2、NaCl、AgNO3、H2SO4四种无色溶液 |
| C、将燃烧的镁条伸入混合气体,以除去CO2中的N2 |
| D、用硫酸镁和硫酸亚铁混合溶液制摩尔盐的过程:蒸发浓缩→冷却结晶→抽滤→用水洗涤2-3次 |
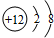 ,该离子的符号为
,该离子的符号为