题目内容
12.相同质量的NO2和N2O4,它们之间的关系正确的是( )| A. | 体积之比为2:1 | B. | 原子总数之比为1:2 | ||
| C. | 物质的量之比为1:1 | D. | 氧原子的个数之比为1:1 |
分析 先设出物质的质量均为46g,利用n=$\frac{m}{M}$来计算和NO2和N2O4的物质的量,
A.体积之比等于物质的量之比;
B.结合分子含有原子数目计算判断;
C.利用n=$\frac{m}{M}$来计算和NO2和N2O4的物质的量;
D.根据分子的组成求氧原子数目之比.
解答 解:设和NO2和N2O4的质量均为46g,则NO2的物质的量为$\frac{46g}{46g/mol}$=1mol,N2O4的物质的量为$\frac{46g}{92g/mol}$=0.5mol,
A.NO2和N2O4所含分子物质的量之比为1mol:0.5mol=2:1,所以体积之比为2:1,故A正确;
B.NO2和N2O4所含原子物质的量之比为1mol×3:0.5mol×6=1:1,故B错误;
C、NO2和N2O4所含分子物质的量之比为1mol:0.5mol=2:1,故C错误;
D、氧原子的个数之比为1mol×2:0.5mol×4=1:1,故D正确;
故选AD.
点评 本题考查物质的量的相关计算,比较基础,注意分子与含有原子之间的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.下列叙述正确的是( )
| A. | 常温下,pH值等于14与pH值等于12的两种NaOH溶液等体积混和后,c(H+)=$\frac{1{0}^{-14}+1{0}^{-10}}{2}$ | |
| B. | 常温下,浓度为1×10-10mol/L的KOH溶液的pH值最接近于4 | |
| C. | 氨水加水稀释,溶液中除水以外的所有粒子的浓度都减小 | |
| D. | 常温下,相同温度下pH值等于1的盐酸溶液中水的电离程度与pH值等于13的Ba(OH)2溶液中水的电离程度相等 |
3.下列各种情况下一定能大量共存的离子组为( )
| A. | pH=7的溶液中:Fe3+、Cl-、Na+、NO3- | |
| B. | 由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、CO32-、Cl-、K+ | |
| C. | pH=1的溶液中:NH4+、Cl-、Cu2+、SO42- | |
| D. | 无色溶液中:Al3+、HCO3-、I-、K+ |
7.下列叙述不正确的是( )
| A. | 溶解性:Na2CO3>NaHCO3 | |
| B. | 热稳定性:Na2CO3>NaHCO3 | |
| C. | 与足量稀盐酸反应:Na2CO3比NaHCO3更剧烈 | |
| D. | 等质量的Na2CO3和NaHCO3分别与足量稀盐酸反应:Na2CO3放出的CO2更多 |
4.下列物质中,不属于电解质溶液的是( )
| A. | 蔗糖溶液 | B. | 硫酸溶液 | C. | 氢氧化钠溶液 | D. | 食盐溶液 |
1.有两种烃,甲为 ,乙为
,乙为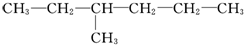 .下列有关它们命名的说法正确的是( )
.下列有关它们命名的说法正确的是( )
 ,乙为
,乙为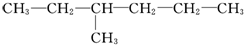 .下列有关它们命名的说法正确的是( )
.下列有关它们命名的说法正确的是( )| A. | 甲、乙的主链碳原子数都是6个 | B. | 甲、乙的主链碳原子数都是5个 | ||
| C. | 甲的名称为2-丙基-1-丁烯 | D. | 乙的名称为3-甲基己烷 |
2.下列反应的离子方程式书写正确的是( )
| A. | 用小苏打治疗胃酸过多:CO3-+2H+═CO2↑+H2O | |
| B. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 硫酸铜溶液中加入过量铁粉:Cu2++2Fe═2Fe3++Cu | |
| D. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO${\;}_{2}^{-}$+H2O |