题目内容
11.12.4g Na2R中含Na+0.4mol,则12.4g Na2R的物质的量为0.2mol,摩尔质量为62g/mol.分析 根据Na原子守恒得n(Na2R),再根据M=$\frac{m}{n}$计算其摩尔质量.
解答 解:根据Na原子守恒得n(Na2R)=$\frac{1}{2}$n(Na+)=$\frac{1}{2}$×0.4mol=0.2mol,M(Na2R)=$\frac{m}{n}$=$\frac{12.4g}{0.2mol}$=62g/mol,
故答案为:0.2;62g/mol.
点评 本题考查物质的量有关计算,侧重考查学生对基本公式的灵活运用,明确各个物理量之间的关系式是解本题关键,注意M单位要书写,为易错点.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
1.一定温度下,在三个体积均为0.5L的恒容密闭容器中发生反应:CO(g)+Cl2(g)?COCl2(g),其中容器Ⅰ中5min时到达平衡.
下列说法中正确的是( )
| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
| CO | Cl2 | COCl2 | COCl2 | ||
| Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
| Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
| Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
| A. | 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol•L-1•min-1 | |
| B. | 该反应正反应为吸热反应 | |
| C. | 容器Ⅱ中起始时Cl2的物质的量为0.55 mol | |
| D. | 若起始时向容器Ⅰ加入CO 0.8 mol、Cl2 0.8 mol,达到平衡时CO转化率小于80% |
2.在100℃时,将0.40mol NO2气体充入2L的密闭容器中,发生如下反应:2NO2(g)?N2O4(g)△H<0.监测反应获得如表数据:下列说法正确的是( )
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A. | 0~20 s内,v(NO2)=0.005 mol•L-1•s-1 | |
| B. | 59 s时,c(NO2)一定大于0.12 mol•L-1 | |
| C. | 若仅将起始时充入NO2的量增至0.80 mol,则该反应的平衡常数K>$\frac{25}{9}$ | |
| D. | 若上述反应在120℃时进行,则反应至80 s时,n(N2O4)<0.08 mol |
19.某温度下,向2L恒容密闭容器中充入1.0mol A和1.0mol B,发生反应:A(g)+B(g)?C(g)经过一段时间后达到平衡.反应过程中测定的部分数据见表,下列说法正确的是( )
| t/s | 0 | 5 | 10 | 20 | 30 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A. | 反应在前5 s的平均速率v(A)=0.03 mol•L-1•s-1 | |
| B. | 达到平衡时,B的转化率为80% | |
| C. | 相同温度下,若起始时向容器中充入2.0 mol C,则达到平衡时C的浓度小于0.2 mol•L-1 | |
| D. | 相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v(正)<v(逆) |
6.某原子含有6个电子、7个中子,它的化学符号为( )
| A. | 13C | B. | 13Al | C. | 13C | D. | 13Al |
16.下列有关的方程式不正确的是( )
| A. | 测0.1 mol/L氨水的pH为11:NH3•H2O?NH4++OH- | |
| B. | 水滴石穿:CO2+CaCO3+H2O═Ca(HCO3)2 | |
| C. | NH4Cl溶解在T2O中:NH4++T2O?NH3•T2O+H+ | |
| D. | 乙烷的燃烧热为-1559.9 kJ•mol-1,则乙烷燃烧的热化学方程式可表示为:2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=-3119.8kJ•mol-1 |
3.进行化学实验必须注意安全,下列说法不正确的是( )
| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌 | |
| D. | 实验室中酒精燃烧,小面积着火,立即用水扑灭 |
20.下列说法正确的是( )
| A. | 28 g氮气含有的原子数为NA | |
| B. | 4g金属钙的物质的量为1mol | |
| C. | 1 mol O2分子的质量等于1 mol氧原子的质量 | |
| D. | 24 g O2分子和24 g O3分子所含的氧原子数目相等 |
4.电镀污泥中包含大量难以降解的贵重金属离子,如Zn2+、Pb2+、Fe2+、Fe3+、Cr3+、Ca2+等.在回收过程中,如果对其处理不当或者未经处理就进行填埋,将会给环境和社会带来极大的危害.以下是回收流程:
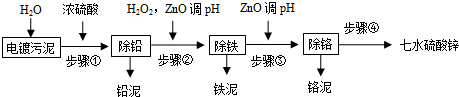
已知:
①各离子开始沉淀和完全沉淀的pH值如下表:
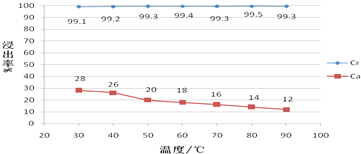
②温度对各离子的浸出率影响如图:
(1)请写出步骤①除铅的离子方程式:Pb2++SO42-=PbSO4↓.
(2)步骤②加入双氧水的离子反应方程式是2Fe2++H2O2+2H+=2Fe3++2H2O,调pH的范围是3.2~3.9.
(3)步骤③加入ZnO调pH的原理是(用离子方程式表示)Cr3++3H2O?Cr(OH)3+3H+、ZnO+2H+=Zn2++H2O;铬泥的主要成分是Cr(OH)3.
(4)步骤④的操作方法是蒸发浓缩、冷却结晶、洗涤、干燥.
(5)由图可以看出在硫酸浸出Ca2+、Cr3+离子的过程中,Ca2+离子浸出率随温度的升高而减小,其原因是硫酸钙是微溶物且溶解度超过30℃以后,温度越高,溶解度越低,Cr3+离子浸出率受温度影响较小,可在常温下浸出,但在实验过程中为了降低溶液的黏度,改善浸出液的过滤性能,浸出液的温度维持在40-50℃,浸出流程中虽然没有加热设备,但仍能使浸出液保持在40-50℃的原因是浓硫酸稀释过程中会放出大量的热,浸出渣的主要成分是硫酸铅、硫酸钙.

已知:
①各离子开始沉淀和完全沉淀的pH值如下表:
| 离子 | Fe2+ | Fe3+ | Cr3+ | Zn2+ |
| 开始沉淀的pH值 | 5.9 | 2.3 | 3.9 | 5.7 |
| 完全沉淀的pH值 | 8.3 | 3.2 | 5.6 | 8.3 |

(1)请写出步骤①除铅的离子方程式:Pb2++SO42-=PbSO4↓.
(2)步骤②加入双氧水的离子反应方程式是2Fe2++H2O2+2H+=2Fe3++2H2O,调pH的范围是3.2~3.9.
(3)步骤③加入ZnO调pH的原理是(用离子方程式表示)Cr3++3H2O?Cr(OH)3+3H+、ZnO+2H+=Zn2++H2O;铬泥的主要成分是Cr(OH)3.
(4)步骤④的操作方法是蒸发浓缩、冷却结晶、洗涤、干燥.
(5)由图可以看出在硫酸浸出Ca2+、Cr3+离子的过程中,Ca2+离子浸出率随温度的升高而减小,其原因是硫酸钙是微溶物且溶解度超过30℃以后,温度越高,溶解度越低,Cr3+离子浸出率受温度影响较小,可在常温下浸出,但在实验过程中为了降低溶液的黏度,改善浸出液的过滤性能,浸出液的温度维持在40-50℃,浸出流程中虽然没有加热设备,但仍能使浸出液保持在40-50℃的原因是浓硫酸稀释过程中会放出大量的热,浸出渣的主要成分是硫酸铅、硫酸钙.