题目内容
甲烷、丙烷和乙烯三种气体混合后密度与同温同压下CO的密度相同,混合气体中甲烷和丙烷的体积比是( )
| A、2:1 | B、4:3 |
| C、1:1 | D、不确定 |
考点:有关混合物反应的计算
专题:计算题
分析:根据在同温同压下密度相同,则物质的相对分子质量也相等,所以甲烷、丙烷和乙烯的平均摩尔质量为28g/mol,乙烯的摩尔质量为28g/mol,则甲烷和丙烷的平均摩尔质量一定为28g/mol,据此进行解答.
解答:
解:甲烷的化学式为:CH4,其相对分子质量为:12+1×4=16;丙烷的化学式为:C3H8,其相对分子质量为:12×3+1×8=44;乙烯的化学式为:C2H4,其相对分子质量为:12×2+1×4=28;CO的相对分子量为28,
相同条件下气体的密度与摩尔质量成正比,则甲烷、丙烷和乙烯的混合气体的平均摩尔质量为28g/mol,
由于乙烯的摩尔质量为28g/mol,则乙烯含量不影响平均摩尔质量,关键是甲烷和丙烷的平均摩尔质量为28g/mol,
设甲烷的物质的量为x、丙烷的物质的量为y,
则
=28,
解得x:y=4:3,
故选B.
相同条件下气体的密度与摩尔质量成正比,则甲烷、丙烷和乙烯的混合气体的平均摩尔质量为28g/mol,
由于乙烯的摩尔质量为28g/mol,则乙烯含量不影响平均摩尔质量,关键是甲烷和丙烷的平均摩尔质量为28g/mol,
设甲烷的物质的量为x、丙烷的物质的量为y,
则
| 16x+44y |
| x+y |
解得x:y=4:3,
故选B.
点评:本题考查了有关混合物的计算,题目难度中等,明确相同条件下气体的摩尔质量与密度成正比为解答本题的关键,注意平均摩尔质量在化学计算中的应用方法.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
某气体混合物由H2、N2、CO和CH4中的一种或两种组成,将该混合气体点燃后的产物依次通过浓H2SO4和NaOH溶液,结果两溶液的质量均有增加.则该混合气体的组成不可能是( )
| A、N2和CO |
| B、H2和CO |
| C、CH4 |
| D、H2和CH4 |
化学与人类生活、社会可持续发展密切相关.下列说法正确的是( )
| A、大量使用化肥和农药,以提高农作物产量 |
| B、用CO2合成聚碳酸醋可降解塑料,实现“碳“的循环利用 |
| C、“天宫一号“使用的碳纤维,是一种新型有机高分子材料 |
| D、为改善食品的色、香、味并防止变质,可加入大量食品添加剂 |
下列各组物质中的四种物质,用一种试剂即可鉴别的是( )
| A、甲酸、乙醛、甲酸钠溶液、乙酸乙酯 |
| B、丙烯、甲烷、乙炔、乙烯 |
| C、苯酚、乙醇、苯、四氯化碳 |
| D、苯乙烯、苯酚、乙苯、二甲苯 |
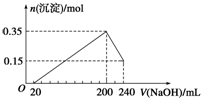 Ⅰ.粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.取适量A进行铝热反应,产物中有单质B生成;请填空:
Ⅰ.粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.取适量A进行铝热反应,产物中有单质B生成;请填空: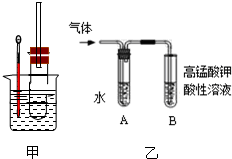 某学习小组用乙醇与氢溴酸为原料制备溴乙烷.该反应发生的原理为:C2H5OH+HBr
某学习小组用乙醇与氢溴酸为原料制备溴乙烷.该反应发生的原理为:C2H5OH+HBr