题目内容
如图是元素周期表的一部分,表中的①-⑩中元素,用化学用语填空回答:
(1)在这些元素中,⑩原子的原子结构示意图为 .
(2)写出①的最高价氧化物和②的单质的电子式 , .
(3)用电子式表示③与④形成化合物的过程 .
(4)①的单质和⑥的氧化物反应的化学方程式 .
(5)写出⑤的单质与氢氧化钠反应的化学方程式: ,写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式: .
(6)已知拆开l mol C-H键、l mol O=O键、l molC=O键、l mol H-O键分别需要吸收的能量为414kJ、498kJ、728kJ、464kJ.则l mol甲烷完全燃烧放出 kJ的热量.
| 族 周期 | I A | IIA | IIIA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ | ⑩ |
(2)写出①的最高价氧化物和②的单质的电子式
(3)用电子式表示③与④形成化合物的过程
(4)①的单质和⑥的氧化物反应的化学方程式
(5)写出⑤的单质与氢氧化钠反应的化学方程式:
(6)已知拆开l mol C-H键、l mol O=O键、l molC=O键、l mol H-O键分别需要吸收的能量为414kJ、498kJ、728kJ、464kJ.则l mol甲烷完全燃烧放出
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置,可知①为C、②为N、③为F、④为Mg、⑤为Al、⑥为Si、⑦为Cl、⑧为Ar,⑨为K、⑩为Br.
(1)⑩是Br元素,原子核内有35个质子,核外有4个电子层,各层电子数为2、8、18、7;
(2)①的最高价氧化物是CO2,分子中C原子与氧原子之间形成2对共用电子对;②的单质是N2,分子中N原子之间形成3对共用电子对;
(3)③与④形成化合物是MgF2,属于离子化合物,Mg失去2个电子成为镁离子,F得到1个电子成为氟离子;
(4)①的单质和⑥的氧化物反应即C与二氧化硅高温下发生置换反应生成Si与CO;
(5)⑤是Al,与氢氧化钠反应生成偏铝酸钠与氢气;氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,氢氧化铝是难溶物,书写离子方程式时不能拆开;
(6)甲烷与氧气燃烧的化学方程式为:CH4+2O2
CO2+2H2O,根据反应热=反应物键能之和-生成物键能之和,据此计算该反应反应热进行解答.
(1)⑩是Br元素,原子核内有35个质子,核外有4个电子层,各层电子数为2、8、18、7;
(2)①的最高价氧化物是CO2,分子中C原子与氧原子之间形成2对共用电子对;②的单质是N2,分子中N原子之间形成3对共用电子对;
(3)③与④形成化合物是MgF2,属于离子化合物,Mg失去2个电子成为镁离子,F得到1个电子成为氟离子;
(4)①的单质和⑥的氧化物反应即C与二氧化硅高温下发生置换反应生成Si与CO;
(5)⑤是Al,与氢氧化钠反应生成偏铝酸钠与氢气;氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,氢氧化铝是难溶物,书写离子方程式时不能拆开;
(6)甲烷与氧气燃烧的化学方程式为:CH4+2O2
| ||
解答:
解:由元素在周期表中位置,可知①为C、②为N、③为F、④为Mg、⑤为Al、⑥为Si、⑦为Cl、⑧为Ar,⑨为K、⑩为Br.
(1)⑩是Br元素,原子核内有35个质子,原子结构示意图为 ,
,
故答案为: ;
;
(2)①的最高价氧化物是CO2,电子式为 ;②的单质是N2,电子式为
;②的单质是N2,电子式为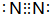 ,
,
故答案为: ;
;
(3)③与④形成化合物是MgF2,属于离子化合物,Mg失去2个电子成为镁离子,F得到1个电子成为氟离子,用电子式表示其形成过程是: ,
,
故答案为: ;
;
(4)①的单质和⑥的氧化物反应即C与二氧化硅高温下发生置换反应,化学方程式为:2C+SiO2
Si+2CO↑,
故答案为:2C+SiO2
Si+2CO↑;
(5)⑤是Al,与氢氧化钠反应的化学方程式为:2Al+2H2O+NaOH=2NaAlO2+3H2↑;氢氧化铝与氢氧化钠溶液反应的离子方程式为:Al(OH)3+OH-=AlO-2+2H2O,
故答案为:2Al+2H2O+NaOH=2NaAlO2+3H2↑;Al(OH)3+OH-=AlO-2+2H2O;
(6)甲烷与氧气燃烧的化学方程式为:CH4+2O2
CO2+2H2O,根据反应热与化学键键能的关系,△H=(4×414+2×498-2×728-2×2×464)kJ/mol=-660 kJ/mol,所以1mol甲烷完全燃烧放出660kJ的热量,故答案为:660.
(1)⑩是Br元素,原子核内有35个质子,原子结构示意图为
 ,
,故答案为:
 ;
;(2)①的最高价氧化物是CO2,电子式为
 ;②的单质是N2,电子式为
;②的单质是N2,电子式为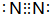 ,
,故答案为:
 ;
;(3)③与④形成化合物是MgF2,属于离子化合物,Mg失去2个电子成为镁离子,F得到1个电子成为氟离子,用电子式表示其形成过程是:
 ,
,故答案为:
 ;
;(4)①的单质和⑥的氧化物反应即C与二氧化硅高温下发生置换反应,化学方程式为:2C+SiO2
| ||
故答案为:2C+SiO2
| ||
(5)⑤是Al,与氢氧化钠反应的化学方程式为:2Al+2H2O+NaOH=2NaAlO2+3H2↑;氢氧化铝与氢氧化钠溶液反应的离子方程式为:Al(OH)3+OH-=AlO-2+2H2O,
故答案为:2Al+2H2O+NaOH=2NaAlO2+3H2↑;Al(OH)3+OH-=AlO-2+2H2O;
(6)甲烷与氧气燃烧的化学方程式为:CH4+2O2
| ||
点评:本题考查元素周期表的应用、元素的性质应用、化学用语的表示、反应热的计算等,难度中等,侧重考查学生对知识的迁移应用,注意掌握用电子式表示化学键或物质的形成.

练习册系列答案
相关题目
下列物质所对应的化学式不正确的是( )
| A、干冰--CO2 |
| B、硫化亚铁--FeS2 |
| C、苏打--Na2CO3 |
| D、重晶石--BaSO4 |
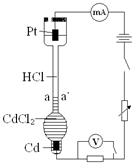 设计如下装置探究HCl溶液中阴、阳离子在电场中的相对迁移速率(已知:Cd的金属活动性大于Cu).恒温下,在垂直的玻璃细管内,先放CdCl2溶液及显色剂,然后小心放入HCl溶液,在aa′处形成清晰的界面.通电后,可观察到清晰界面缓缓向上移动.下列说法正确的是( )
设计如下装置探究HCl溶液中阴、阳离子在电场中的相对迁移速率(已知:Cd的金属活动性大于Cu).恒温下,在垂直的玻璃细管内,先放CdCl2溶液及显色剂,然后小心放入HCl溶液,在aa′处形成清晰的界面.通电后,可观察到清晰界面缓缓向上移动.下列说法正确的是( )| A、通电时,H+、Cd2+向Cd电极迁移,Cl-向Pt电极迁移 | ||||
| B、一定时间内,如果通过HCl溶液某一界面的总电量为1.0 C,测得H+所迁移的电量为0.82 C,说明该HCl溶液中H+的迁移速率约是Cl-的4.6倍 | ||||
| C、如果电源正负极反接,则下端产生大量Cl2,使界面不再清晰,实验失败 | ||||
D、装置中总反应的化学方程式为:2HCl
|
下列关于电解质溶液中离子浓度关系的说法正确的是( )
| A、0.1mol/L的NaHCO3溶液中离子浓度的关系:c(Na+)═c(HCO3-)+c(H2CO3)+2c(CO32-) |
| B、0.1mol/L的NH4Cl溶液和0.1mol/L的NH3?H2O等体积混合后离子浓度的关系:c(NH4+)>c( Cl-)>c(OH-)>c(H+) |
| C、常温下,物质的量浓度相等的醋酸溶液与氢氧化钠溶液等体积混合,所得溶液PH=7 |
| D、KHS溶液中存在等式关系:c(S2-)+c(OH-)=c(H+)+c(H2S) |
在隔绝空气的情况下,9.8g铁镁铝混合物溶解在一定量某浓度的稀硝酸中,当金属完全溶解后收集到4.48L(标准状况下)NO气体.在反应后的溶液中加入足量的烧碱溶液,可生成氢氧化物沉淀的质量可能为( )
| A、18g | B、20g |
| C、22g | D、24g |
向2L密闭容器中加入2molNH3和3molO2发生反应4NH3(g)+5O2(g))=4NO(g)+6H2O(g)半分钟后,测的NH3剩余1mol,下列说法不正确的是( )
| A、该反应生成了1.5mol的水蒸气 |
| B、用O2表示该反应速率为2.5mol/(L?min) |
| C、反应后容器中NO的浓度为0.5mol/L |
| D、反应后容器中n(NH3)=n(NO) |
现有200mL MgCl2和AlCl3的混合溶液,其中c(Mg2+)=0.2mol/L,c(Cl-)=1.3mol/L,要使Mg2+转化成Mg(OH)2,并使Mg2+、Al3+分离开来,4mol/L NaOH溶液的最少用量为( )
| A、140mL | B、120mL |
| C、100mL | D、80mL |
下列各组混合物无论以何种比例混合,只要总的物质的量一定,完全燃烧时消耗氧气的量是定值的是( )
| A、CH2=CH2、C2H5OH、HOCH2CH2COOH |
| B、CH2O、C2H4O2、C6H12O6 |
| C、C6H6、C5H10、C6H6O |
| D、H2、CO、CH3OH |