题目内容
在NaCl、MgSO4、MgCl2和三种盐配成的混合溶液中,若Na+的浓度为0.1mol/L、Mg2+的浓度为0.25mol/L、Cl-的浓度为0.2mol/L,则SO42-的物质的量浓度为( )
| A、0.5mol?L-1 |
| B、0.45mol?L-1 |
| C、0.2mol?L-1 |
| D、0.25mol?L-1 |
考点:物质的量浓度的相关计算
专题:
分析:设硫酸根的物质的量浓度为c,根据溶液中阴阳离子所带的正负电荷总数相等,列式计算c值.据此判断.
解答:
解:设硫酸根的物质的量浓度为c,根据溶液中阴阳离子所带的正负电荷总数相等,则:
0.10mol?L-1×1+0.25mol?L-1×2=0.20mol?L-1×1+2c
解得:c=0.2mol/L.
故选:C.
0.10mol?L-1×1+0.25mol?L-1×2=0.20mol?L-1×1+2c
解得:c=0.2mol/L.
故选:C.
点评:本题考查溶液物质的量浓度的计算,难度不大,利用常规解法,比较麻烦,本题根据溶液不显电性阳离子与阴离子所带电荷总数相等,即电荷守恒原则解答,注意电荷守恒原则在混合溶液有关离子浓度计算经常运用.

练习册系列答案
相关题目
下列反应中必须加入还原剂才能进行的是( )
| A、O2→OH- |
| B、Zn→Zn2+ |
| C、H2→H2O |
| D、CuO→CuCl2 |
按照原子核外电子排布规律:各电子层最多容纳的电子数为2n2(n为电子层数,其中,最外层电子数不超过8个,次外层不超过18个).1999年已发现了核电荷数为118的元素,其原子核外电子层排布是( )
| A、2,8,18,32,32,18,8 |
| B、2,8,18,32,50,8 |
| C、2,8,18,32,18,8 |
| D、2,8,18,32,50,18,8 |
将5mol?L-1盐酸10mL稀释到200mL,再取出5mL,这5mL溶液的物质的量浓度是( )
| A、0.05 mol?L-1 |
| B、0.25 mol?L-1 |
| C、0.1 mol?L-1 |
| D、0.5 mol?L-1 |
下列离子方程式书写正确的是( )
| A、向明矾溶液加入过量氨水:Al3++4OH-═〔Al(OH)4〕- |
| B、碳酸钙溶于稀盐酸:CO32-+2H+═H2O+CO2↑ |
| C、SO2通入足量的Ba(NO3)2稀溶液中:3SO2+2H2O+2NO3-+3Ba2+═3BaSO4↓+2NO+4H+ |
| D、一小块钠投入到CuSO4溶液中:2Na+Cu2+═Cu+2Na+ |
关于 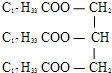 ,下列说法正确的是( )
,下列说法正确的是( )
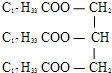 ,下列说法正确的是( )
,下列说法正确的是( )| A、属于油脂,名为硬脂酸甘油酯 |
| B、常温下呈固态 |
| C、属于高分子化合物 |
| D、碱性条件下能发生皂化反应 |
在标准状况下,气体A的密度为1.25g/L,气体B的相对分子质量为42,A和B的混合气体在相同状况下对H2的相对密度为16.8,则混合气体中A和B的体积比为( )
| A、3:2 | B、2:1 |
| C、2:3 | D、1:2 |
下列变化中,一定需加还原剂才能实现的是( )
| A、CO2→CO32- |
| B、FeCl3→FeCl2 |
| C、C→CO2 |
| D、KMnO4→MnO2 |