题目内容
15.化学与生活密切相关,下列说法正确的是( )| A. | 绿色化学的核心就是治理工业生产对环境产生的污染 | |
| B. | 铁、钙、碘都是人体必不可少的微量元素 | |
| C. | 食盐可作调味剂,但不可作食品防腐剂 | |
| D. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
分析 A、绿色化学的核心是提高原子利用率,减少污染;
B、钙不是微量元素;
C、食盐具有咸味,常用作调味品和防腐剂;
D、“地沟油”的成分是油脂.
解答 解:A、绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染,而不是产生污染再治理,故A错误;
B、钙不是微量元素,钙在人体内是常量元素,故B错误;
C、食盐可以做食品的防腐剂,如用食盐来腌制食品能防止腐烂,故C错误;
D、“地沟油”的成分是油脂,可用来制肥皂和生物柴油,故D正确;
故选D.
点评 本题考查了食品添加剂、微量元素、绿色化学等概念,涉及知识面广,难度不大,注意基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列互为同位素的是( )
| A. | H2O和D2O | B. | H2和D2 | C. | ${\;}_{1}^{1}H$和${\;}_{1}^{2}H$ | D. | H2O和H2O2 |
3.现取mg镁铝合金在一定浓度的稀硝酸中恰好完全溶解(硝酸的还原产物只有NO),向反应后的混合溶液中滴加bmol/LNaOH溶液,当滴加到VmL时,得到沉淀质量恰好为最大值ng,则下列有关该说法中不正确的有( )
| A. | 标准状况下生成N的体积为$\frac{22.4(n-m)}{51}$L | |
| B. | 沉淀中OH-的质量为17bVg | |
| C. | 恰好溶解后溶液中的NO3-的物质的量为$\frac{bV}{1000}$mol | |
| D. | 与合金反应的硝酸的物质的量为($\frac{n-m}{51}$+$\frac{bV}{1000}$)mol |
10.下列实验操作可以达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 配制银氨溶液 | 向3mL2%的AgNO3溶液中滴入2滴2%的氨水 |
| B | 分离提纯鸡蛋清中的蛋白质 | 向鸡蛋清溶液中加入醋酸铅溶液,充分振荡后过滤,将不溶物加入蒸馏水中 |
| C | 检验蔗糖水解溶液的还原性 | 取2mL 20%的蔗糖溶液,加入少量稀硫酸,水浴后取少量溶液,加入几滴新制Cu(OH)2,加热 |
| D | 检验溴乙烷在NaOH溶液中是否发生水解 | 将溴乙烷与NaOH溶液共热.冷却后,取出上层溶液,用稀硝酸酸化,加入AgNO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
20.下列说法正确的是( )
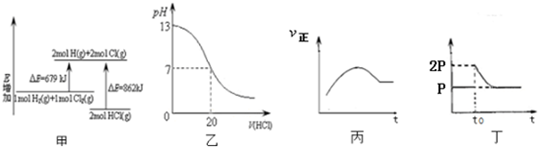

| A. | 图甲表示H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=+183 kJ/mol | |
| B. | 图乙表示室温时用0.1 mol/L盐酸滴定20 mL 0.1 mol/LNaOH溶液,溶液pH变化 | |
| C. | 图丙表示向恒容绝热的密闭容器中通入A和B,发生2A (g)+B (g)?2C(g)反应,其正反应速率随时间变化的示意图,则该反应为吸热反应 | |
| D. | 图丁表示在恒温密闭容器中,2BaO2(s)?2BaO(s)+O2(g)达到平衡,t0时刻将容器体积缩小为原来的1/2,体系重新达到平衡过程体系压强的变化 |
7.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 24克金刚石中含有的碳碳键数目为4NA | |
| B. | 50mL18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| C. | 1L1mol•L-1饱和FeCl3溶液滴入沸水中完全水解生成Fe(OH)3胶体粒子数为NA | |
| D. | 120克熔融的NaHSO4中含有的离子数为3NA |
4.下列指定反应的离子方程式正确的是( )
| A. | NO2溶于水:3NO2+H2O=H++NO3-+2NO | |
| B. | NaClO溶液中ClO-的水解:ClO-+H2O=HClO+OH- | |
| C. | 酸性条件下,用H2O2将I-转化为I2:H2O2+2I-+2H+=I2+2H2O | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O |
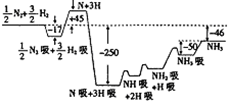 2007年度诺贝尔化学奖获得者格哈德•埃特尔建立了合成氨反应机理,T=673K时,各步反应的能量变化如图所示,图中的能量单位为kJ•mol-1.(注:图中“吸”表示在催化剂表面的吸附)请回答下列问题:
2007年度诺贝尔化学奖获得者格哈德•埃特尔建立了合成氨反应机理,T=673K时,各步反应的能量变化如图所示,图中的能量单位为kJ•mol-1.(注:图中“吸”表示在催化剂表面的吸附)请回答下列问题: