题目内容
 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.(1)根据下表中数据,在画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
(3)列式计算该反应在0-3min时间内产物Z的平均反应速率:
(4)列式计算该反应在0-5min时间内反应物Y的转化率:
(5)该反应达到平衡时反应物X的转化率等于
(6)如果该反应是放热反应.改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如图所示).则曲线1、2、3所对应的实验条件改变分别是:曲线1
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:由表中数据可知,X、Y为反应物,Z为生成物,1min时△n(X)=1mol-0.9mol=0.1mol,△n(Y)=1mol-0.8mol=0.2mol,△n(Z)=0.2mol,9min后各物质的物质的量不再变化,且反应物不为0,故为可逆反应,物质的量变化量之比等于化学计量数之比,故反应方程式为X+2Y 2Z.
2Z.
(1)根据X、Z的物质的量(n)随时间(t)变化画出变化曲线;
(2)根据物质的量的变化与化学计量数呈正比书写化学方程式;
(3)根据v=
计算Z的反应速率;
(4)根据转化率=
×100%计算Y的转化率;
(5)根据转化率=
×100%计算平衡时X的转化率,根据产率=
×100%计算平衡时Z的产率,平衡时Y的体积分数=
×100%计算Y的体积分数;
(6)根据平衡是Z的物质的量的变化,结合反应正反应为放热反应,且为气体体积增大的反应.分析平衡的移动,进而判断改变的条件.
 2Z.
2Z.(1)根据X、Z的物质的量(n)随时间(t)变化画出变化曲线;
(2)根据物质的量的变化与化学计量数呈正比书写化学方程式;
(3)根据v=
| △c |
| △t |
(4)根据转化率=
| 转化了的物质的量 |
| 起始总物质的量 |
(5)根据转化率=
| 转化了的物质的量 |
| 起始总物质的量 |
| 实际产量 |
| 理论产量 |
| 平衡时Y的物质的量 |
| 平衡时体系气体总物质的量 |
(6)根据平衡是Z的物质的量的变化,结合反应正反应为放热反应,且为气体体积增大的反应.分析平衡的移动,进而判断改变的条件.
解答:
解:(1)由表中数据可知,X、Y为反应物,Z为生成物,1min时△n(X)=1mol-0.9mol=0.1mol,△n(Y)=1mol-0.8mol=0.2mol,△n(Z)=0.2mol,所以X、Y、Z在相同时间内的变化量之比为1:2:2,9min后各物质的物质的量不再变化,平衡时X、Y、Z的物质的量分别为:0.55mol、0.1mol、0.9mol.
横坐标为时间,从坐标为X、Z的物质的量(n),根据表中数据可画出曲线为: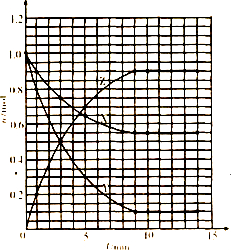 ,
,
故答案为: ;
;
(2)由表中数据看出反应从开始到平衡,X的物质的量减小,应为反应物,0~1min物质的量变化值为1.00mol-0.90mol=0.10mol,Y的物质的量减小,应为反应物,0~1min物质的量变化值为1.00mol-0.80mol=0.20mol,Z的物质的量增多,应为是生成物,物质的量的变化值为0.20mol,9min后各物质的物质的量不再变化,且反应物不为0,故为可逆反应,根据物质的量的变化与化学计量数呈正比,则n(X):n(Y):n(Z)=0.10mol:0.20mol:0.20mol=1:2:2,反应方程式为X+2Y 2Z,
2Z,
故答案为:X+2Y 2Z;
2Z;
(3)在0-3min时,△n(Z)=0.5mol,所以v(Z)=
=0.083mol/(L?min),
故答案为:0.083mol/(L?min);
(4)在0-5min时,△n(Y)=0.7mol,所以Y的转化率=
×100%=70%,
故答案为:70%;
(5)该反应达到平衡时,△n(X)=1mol-0.55mol=0.45mol,n(Y)=0.1mol,n(Z)=0.9mol,所以X的转化率=
×100%=45%,假设反应完全正向进行,根据表中数据和方程式可知,生成Z的物质的量为1.0mol,所以Z的产率=
×100%=90%,平衡时混合体系的气体总物质的量为0.55mol+0.1mol+0.9mol=1.55mol,所以Y的体积分数=
×100%=6.5%,
故答案为:45%;90%;6.5%;
(6)该可逆反应正反应为放热反应,且为气体体积增大的反应.
由表中数据可知,平衡时Z的物质的量为0.9mol,由图2可知曲线①平衡后,Z的物质的量为0.6,Z的物质的量减小,故平衡向逆反应移动,应是升高温度;曲线②平衡后,Z的物质的量为0.9mol,Z的物质的量未变,应是使用催化剂;曲线③平衡后,Z的物质的量为0.95mol,Z的物质的量增大,应是增大压强,
故答案为:升高温度;加入催化剂;增大压强.
横坐标为时间,从坐标为X、Z的物质的量(n),根据表中数据可画出曲线为:
 ,
,故答案为:
 ;
;(2)由表中数据看出反应从开始到平衡,X的物质的量减小,应为反应物,0~1min物质的量变化值为1.00mol-0.90mol=0.10mol,Y的物质的量减小,应为反应物,0~1min物质的量变化值为1.00mol-0.80mol=0.20mol,Z的物质的量增多,应为是生成物,物质的量的变化值为0.20mol,9min后各物质的物质的量不再变化,且反应物不为0,故为可逆反应,根据物质的量的变化与化学计量数呈正比,则n(X):n(Y):n(Z)=0.10mol:0.20mol:0.20mol=1:2:2,反应方程式为X+2Y
 2Z,
2Z,故答案为:X+2Y
 2Z;
2Z;(3)在0-3min时,△n(Z)=0.5mol,所以v(Z)=
| ||
| 3min |
故答案为:0.083mol/(L?min);
(4)在0-5min时,△n(Y)=0.7mol,所以Y的转化率=
| 0.7 |
| 1.0 |
故答案为:70%;
(5)该反应达到平衡时,△n(X)=1mol-0.55mol=0.45mol,n(Y)=0.1mol,n(Z)=0.9mol,所以X的转化率=
| 0.45 |
| 1.0 |
| 0.9 |
| 1.0 |
| 0.1 |
| 1.55 |
故答案为:45%;90%;6.5%;
(6)该可逆反应正反应为放热反应,且为气体体积增大的反应.
由表中数据可知,平衡时Z的物质的量为0.9mol,由图2可知曲线①平衡后,Z的物质的量为0.6,Z的物质的量减小,故平衡向逆反应移动,应是升高温度;曲线②平衡后,Z的物质的量为0.9mol,Z的物质的量未变,应是使用催化剂;曲线③平衡后,Z的物质的量为0.95mol,Z的物质的量增大,应是增大压强,
故答案为:升高温度;加入催化剂;增大压强.
点评:本题考查化学平衡移动、外界条件对平衡的影响、化学平衡图象及作图能力等,难度中等,(1)中作图注意起点、平衡时各物质的物质的量以及X、Y、Z在相同时间内的变化量关系.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
下列各组物质不易用物理性质区别的是( )
| A、苯和四氯化碳 |
| B、酒精和汽油 |
| C、碘和高锰酸钾固体 |
| D、氯化铵和硝酸铵晶体 |
下列说法不正确的是( )
| A、合成纤维与人造纤维可以统称为化学纤维 |
| B、酚醛树脂和聚氯乙烯都是热固性塑料 |
| C、天然橡胶的化学组成是聚异戊二烯 |
| D、复合材料一般有强度高、质量轻、耐高温、耐腐蚀等优异性能,其综合性质超过了单一材料 |
将下列各组物质按酸、碱、盐分类顺序排列,正确的是( )
| A、硫酸,纯碱,石灰石 |
| B、醋酸,烧碱,硫酸铜 |
| C、磷酸,熟石灰,苛性钠 |
| D、醋酸,氨水,熟石灰 |
下列溶液中Cl-的物质的量与100mL 2mol?L-1MgCl2溶液中Cl-的物质的量相等的是( )
| A、150 mL 4 mol?L-1 NaCl溶液 |
| B、75 mL 1 mol?L-1 AlCl3溶液 |
| C、50 mL 2 mol?L-1 CaCl2溶液 |
| D、200 mL 2 mol?L-1 KCl溶液 |
 ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.
ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.