题目内容
11.煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、甲醚等广泛用于工农业生产中.(1)已知:①C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3kJ•mol-1②CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41.3kJ•mol-1
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为C(s)+2H2O(g)=CO2(g)+2H2(g)△H=+90.0kJ•mol-1.该反应在高温(填“高温”、“低温”或“任何温度”)下有利于正向自发进行.
分析 (1)根据盖斯定律来写出碳与水蒸气反应生成一氧化碳和氢气的热化学方程式;根据反应能否自发进行的判据(△G=△H-T△S)来回答.
解答 解:(1)已知①C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3kJ•mol-1
②CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41.3kJ•mol-1
根据盖斯定律,将①-②可得:C(s)+2H2O(g)=CO2(g)+2H2(g)△H=+90kJ•mol-1,反应的焓变△H>0,△S>0,根据反应自发进行的判据
△G=△H-T△S<0,所以需要高温下发生,
故答案为:C(s)+2H2O(g)=CO2(g)+2H2(g)△H=+90.0 kJ•mol-1;高温.
点评 本题考查热化学方程式的书写,以及用△G=△H-T△S来判断反应能否自发进行,本题难度中等.

练习册系列答案
相关题目
7.由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.
①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如下离子的溶液.
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象).阳极上发生的电极反应为2Cl--2e-=Cl2↑、4OH--4e-=2H2O+O2↑;阴极收集到的气体体积为(标准状况)6.72L.
①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如下离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/(mol•L-1) | 0.5 | 2 | 2 | 0.5 |
16.C8H8O2能与NaOH溶液反应,其苯环的一元取代物的种数为( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
20.下列说法正确的是( )
| A. | SO2使品红、酸性高锰酸钾溶液褪色,均体现SO2的漂白性 | |
| B. | 完全由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 元素周期表有18列,就有18个族 | |
| D. | SO2的水溶液能导电,所以SO2是电解质 |
1.下列说法错误的是( )
| A. | 有机物均易燃烧 | |
| B. | 苯酚酸性比碳酸弱,故苯酚不能与碳酸钠溶液反应 | |
| C. | 制取乙酸乙酯时,试剂的混合顺序是先加浓硫酸,再加乙醇,然后加乙酸 | |
| D. | 石油分馏得到的汽油是纯净物 |
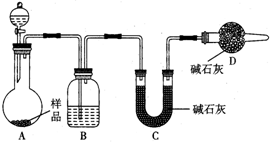 为测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案:
为测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案: