题目内容
下物质分类组合正确的是( )
| A | B | C | D | |
| 强电解质 | HBr | FeCl3 | H3PO4 | Ca(OH)2 |
| 弱电解质 | HF | CH3COOH | BaSO4 | HI |
| 非电解质 | NH3 | Cu | H2O | C2H5OH |
| A、A | B、B | C、C | D、D |
考点:强电解质和弱电解质的概念,电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物;
在水溶液中完全电离的是强电解质;部分电离的是弱电解质.
非电解质:在熔融状态和水溶液中都不能导电的化合物;
在水溶液中完全电离的是强电解质;部分电离的是弱电解质.
解答:
解:A.HBr在水溶液中完全电离,是强电解质;HF在水溶液中部分电离,是弱电解质;NH3自身不能电离,是非电解质,故A正确;
B.FeCl3在水溶液中完全电离,是强电解质;CH3COOH在水溶液中部分电离,是弱电解质;Cu是单质,既不是电解质也不是非电解质,故B错误;
C.H3PO4在水溶液中部分电离,是弱电解质;BaSO4溶于水的部分完全电离,是强电解质;H2O部分电离,是弱电解质,故C错误;
D.Ca(OH)2溶于水的部分完全电离,是强电解质;HI在水溶液中完全电离,是强电解质;C2H5OH在熔融状态和水溶液中都不能导电,是非电解质,故D错误;
故选A.
B.FeCl3在水溶液中完全电离,是强电解质;CH3COOH在水溶液中部分电离,是弱电解质;Cu是单质,既不是电解质也不是非电解质,故B错误;
C.H3PO4在水溶液中部分电离,是弱电解质;BaSO4溶于水的部分完全电离,是强电解质;H2O部分电离,是弱电解质,故C错误;
D.Ca(OH)2溶于水的部分完全电离,是强电解质;HI在水溶液中完全电离,是强电解质;C2H5OH在熔融状态和水溶液中都不能导电,是非电解质,故D错误;
故选A.
点评:本题重点考查强弱电解质、非电解质概念的辨析,难度不大.要注意强电解质在水溶液中是完全电离的.

练习册系列答案
相关题目
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 如图实验制取少量的Fe(OH)3胶体 |
B、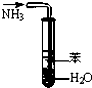 如图实验试管中溶液吸收NH3,并防止倒吸 |
C、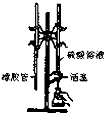 如图实验用H2SO4标准溶液滴定NaOH溶液 |
D、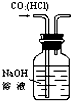 可用如图实验装置除去CO2气体中含有的少量HCl杂质 |
已知:H+H═H2;△H=-436KJ/mol,则下列叙述正确的是( )
①2个H原子的能量高于1个H2的能量
②2个H原子的能量低于1个H2的能量
③H2分子比H原子稳定
④H原子比H2分子稳定.
①2个H原子的能量高于1个H2的能量
②2个H原子的能量低于1个H2的能量
③H2分子比H原子稳定
④H原子比H2分子稳定.
| A、②③ | B、①③ | C、①④ | D、②④ |
英国科学家近日研发出一种名为NOTT-202a的新型多孔材料,空气中其他气体可自由通过这些孔洞,但CO2会被截留.该材料的分子结构单元是以铟原子为中心,周围是以各种有机分子链条编织成的“笼子”,整体上看呈现出多孔特征,有些类似自然界中的蜂窝结构.下列有关说法正确的是( ) 

| A、该材料是一种特殊结构的金属 |
| B、该材料只吸收CO2,其他任何气体都能自由通过 |
| C、该材料吸收22.4LCO2后,增重44g |
| D、该材料可用于工厂的烟囱,吸收CO2,减少碳排放 |
钠硫高能蓄电池的结构如右下图,M为Na2O和Al2O3的混合物,电池的反应原理为2Na+xS?Na2Sx,电池工作温度为320℃.下列说法错误的是( )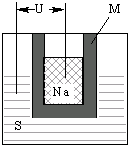

| A、Na电极为电池负极,S电极为电池正极 | ||
B、电池放电时,正极反应为xS+2e-═S
| ||
| C、电池充电时.Na所在电极连接电源正极 | ||
| D、M的作用为导电和隔离钠和硫 |
下列反应中反应物的总能量比生成物低的是( )
| A、盐酸与氢氧化钠反应 |
| B、铁和稀硫酸的反应 |
| C、氢氧化钡晶体的粉末和氯化铵晶体混合 |
| D、木炭在氧气中燃烧 |
关于如图所示的原电池,下列说法正确的是( )
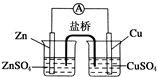

| A、锌电极发生还原反应,铜电极发生氧化反应 |
| B、盐桥中的阴离子向硫酸铜溶液中迁移 |
| C、电子从锌电极通过电流计流向铜电极 |
| D、铜电极上发生的电极反应为2H++2e-═H2↑ |