题目内容
9.苯与一卤代烷在催化剂作用下可生成苯的同系物: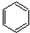 +CH3Cl$\stackrel{AlCl_{3}}{→}$
+CH3Cl$\stackrel{AlCl_{3}}{→}$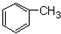 +HCl
+HCl在催化剂存在下,由苯和下列各组物质合成乙苯最好应选用的是( )
| A. | CH3CH3和Cl2 | B. | CH2=CH2和Cl2 | C. | CH2=CH2和HCl | D. | CH3CH3和HCl |
分析 由 +CH3Cl$\stackrel{AlCl_{3}}{→}$
+CH3Cl$\stackrel{AlCl_{3}}{→}$ +HCl可知,合成乙苯需要苯和氯乙烷,而氯乙烷可利用乙烯与HCl加成反应制取,以此来解答.
+HCl可知,合成乙苯需要苯和氯乙烷,而氯乙烷可利用乙烯与HCl加成反应制取,以此来解答.
解答 解:由CH2=CH2+HCl→CH3CH2Cl,
结合信息可知,苯与氯乙烷合成乙苯,
只有选项C中可得到纯净的氯乙烷,
故选:C.
点评 本题考查有机物的合成,注意把握官能团与性质的关系,明确信息及乙烯的加成反应特点是解答的关键,题目难度不大.

练习册系列答案
相关题目
5.类比推理是化学中常用的思维方法.下列推理正确的是( )
| A. | CO2是直线型分子,推测CS2也是直线型分子 | |
| B. | SiH4的沸点高于CH4,推测H2Se的沸点高于H2S | |
| C. | Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3 | |
| D. | NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr |
17.某烃分子中结构含一个苯环、两个碳碳双键和一个碳碳三键,它的分子式可能为( )
| A. | C9H12 | B. | C17H20 | C. | C20H30 | D. | C12H20 |
4.肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.
已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-1 135.7kJ/mol;
下列说法正确的是( )
已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-1 135.7kJ/mol;
下列说法正确的是( )
| A. | N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-1 068 kJ/mol | |
| B. | 肼是与氨类似的弱碱,它易溶于水,其电离方程式:N2H4+H2O═N2H5++OH- | |
| C. | 铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,放电时的负极反应式:N2H4-4e-+4OH-=N2+4H2O | |
| D. | 铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,工作一段时间后,KOH溶液的pH将增大 |
14.在2A+B?3C+4D反应中,表示该反应速率最快的是( )
| A. | v(A)=0.5 mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.8 mol•L-1•s-1 | D. | v(D)=30 mol•L-1•min-1 |
18.下列反应的离子方程式正确是( )
| A. | 向沸水中滴加饱和氯化铁溶液:Fe3++3H2O=Fe(OH)3↓+3H+ | |
| B. | 氯化银溶于浓氨水:AgCl+2NH3•H2O=[Ag(NH3)2]Cl+2H2O | |
| C. | 工业上制取漂白粉:Cl2+2OH-=Cl-+ClO-+H2O | |
| D. | NaNO2溶液中加入酸性高锰酸钾溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
19. 工业上用N2和H2 合成NH3“N2(g)+3H2(g)═2NH3(g)△H<0”,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
工业上用N2和H2 合成NH3“N2(g)+3H2(g)═2NH3(g)△H<0”,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
(1)已知:
N2(g)+O2(g)═2NO(g)△H=+a kJ•mol-1
N2(g)+3H2(g)═2NH3(g)△H=-b kJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H=-c kJ•mol-1
若有34g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为(1.5c-a-b)kJ.
(2)合成NH3达到平衡后,某时刻改变下列条件A,在达到新平衡的过程中正反应速率始终增大.
A.升温 B.加压 C.增大c(N2) D.降低c(NH3)
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响.实验结果如如图1所示:(图中T表示温度,n表示起始时H2物质的量)
①图象中T2和T1的关系是:T2<T1(填“>”、“<”、“=”或“无法确定”).
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是c(填字母).
③若容器容积为1L,b点对应的n=0.15mol,测得平衡时H2的转化率为60%,则平衡时N2的物质的量浓度为0.02 mol•L-1.
(4)一定温度下,将2mol N2和4mol H2置于1L的恒容密闭容器中反应,测得不同条件、不同时间段内合成NH3反应中N2的转化率,得到数据如表:
表中a、b、80%三者的大小关系为80%<a=b或80%<a<b.(填“>”、“=”、“<”、“无法比较”)
(5)向绝热、恒容的密闭容器中通入H2、N2使其在一定条件下合成NH3,请在图2中画出平衡常数K随时间的变化曲线.
 工业上用N2和H2 合成NH3“N2(g)+3H2(g)═2NH3(g)△H<0”,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
工业上用N2和H2 合成NH3“N2(g)+3H2(g)═2NH3(g)△H<0”,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:(1)已知:
N2(g)+O2(g)═2NO(g)△H=+a kJ•mol-1
N2(g)+3H2(g)═2NH3(g)△H=-b kJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H=-c kJ•mol-1
若有34g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为(1.5c-a-b)kJ.
(2)合成NH3达到平衡后,某时刻改变下列条件A,在达到新平衡的过程中正反应速率始终增大.
A.升温 B.加压 C.增大c(N2) D.降低c(NH3)
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响.实验结果如如图1所示:(图中T表示温度,n表示起始时H2物质的量)
①图象中T2和T1的关系是:T2<T1(填“>”、“<”、“=”或“无法确定”).
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是c(填字母).
③若容器容积为1L,b点对应的n=0.15mol,测得平衡时H2的转化率为60%,则平衡时N2的物质的量浓度为0.02 mol•L-1.
(4)一定温度下,将2mol N2和4mol H2置于1L的恒容密闭容器中反应,测得不同条件、不同时间段内合成NH3反应中N2的转化率,得到数据如表:
 | 1小时 | 2 小时 | 3小时 | 4小时 |
| T3 | 30% | 50% | 80% | 80% |
| T4 | 35% | 60% | a | b |
(5)向绝热、恒容的密闭容器中通入H2、N2使其在一定条件下合成NH3,请在图2中画出平衡常数K随时间的变化曲线.
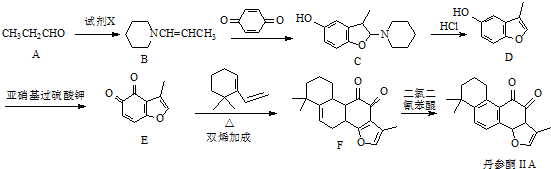
 .
. .
.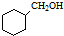 的合成路线流程图(无机试剂可任选).
的合成路线流程图(无机试剂可任选).